
科目: 来源:同步题 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:问答题
| A.18% | B.36% | C.46% | D.53% |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.
| B.(
| ||||||
C.(
| D.
|
查看答案和解析>>
科目: 来源:模拟题 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.4.5g | B.9.9g | C.13.2g | D.14.7g |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.4.18g | B.3.12g | C.4.68g | D.5.08 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.氯化钾既不是氧化产物,也不是还原产物 |
| B.被还原的K35ClO3和被氧化的H37Cl的物质的量之比为1:6 |
| C.生成氯气的相对分子质量为72 |
| D.每生成标准状况下的氯气11.2L,转移电子数为6.02×1023 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 一定条件 |
查看答案和解析>>
科目: 来源:不详 题型:多选题
| A.每生成1 mol Fe3O4,反应转移的电子总数为4 mol? | ||
| B.Fe2+和S2O32-都是还原剂? | ||
C.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为
| ||
| D.x=2? |
查看答案和解析>>
科目: 来源:不详 题型:问答题
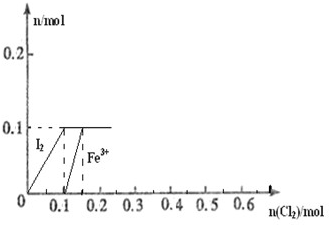
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com