
科目: 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子,其物质的量浓度比为Na+:Mg2+:Cl-=3:5:5,若Na+浓度为3mol/L,则SO42-的浓度为
A.2mol/L B.3mol/L C.4mol/L D.8mol/L
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
为了除去KCl固体中少量MgSO4和CaCl2杂质,须进行下列六项操作,正确的次序是①加水溶解; ②加热蒸发得到晶体; ③加入过量BaCl2溶液; ④加入过量盐酸; ⑤加入过量的K2CO3 ⑥过滤
A.①⑤③⑥④② B.①⑤③④⑥②
C.①③④⑥⑤② D.①③⑤⑥④②
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:填空题
(8分)(1)标准状况下,0.2mol NH3与_________________g H2O的电子数相等。
(2)含有相同氧原子数的CO和CO2,其质量比为_________________________。
(3)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量______________。
(4)已知V mLAl2(SO4)3溶液中含Al3+ a g,则溶液中SO42-的物质的量浓度是____________________。
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:计算题
(8分)向50mL稀硫酸和稀盐酸的混合溶液中,加入3.42g氢氧化钡粉末,充分反应后过滤,得到干燥的沉淀物2.33g,所得溶液中氢氧根离子的浓度为0.1mol/L,试求原混合液中SO42-和Cl-的物质的量浓度(假定在混合液中加入氢氧化钡粉末后体积未改变)。
查看答案和解析>>
科目: 来源:2016届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:
2SO2(g)+ O2(g)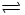 2SO3(g),达到平衡后改变下述条件,SO3(g)的平衡浓度不改变的是
2SO3(g),达到平衡后改变下述条件,SO3(g)的平衡浓度不改变的是
A.保持温度和容器内压强不变,充入1molSO3
B.保持温度和容器体积不变,充入1molSO3
C.保持温度和容器内压强不变,充入1molO2
D.保持温度和容器内压强不变,充入1molAr
查看答案和解析>>
科目: 来源:2016届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是
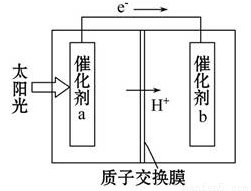
A.该过程是将太阳能转化为化学能的过程
B.催化剂a表面发生氧化反应,有O2产生
C.催化剂a附近酸性减弱,催化剂b附近酸性增强
D.催化剂b表面的反应是CO2 +2H++2e一=HCOOH
查看答案和解析>>
科目: 来源:2016届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
用惰性电极电解含有一定量的下列溶质的溶液,一段时间后,再加入一定质量的另一种物质(中括号内),溶液可能与原来溶液完全一样的是
A.CuCl2[CuSO4] B.NaOH[NaOH]
C.NaCl[HCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目: 来源:2016届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
一定条件下存在反应:C(s)+H2O(g)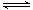 CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
容器 | 甲 | 乙 |
|
容积 | 0.5 L | 0.5 L | V |
温度 | T1 ℃ | T2 ℃ | T1 ℃ |
起始量 | 2 molC1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |
下列说法正确的是
A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L-1·min-1
B.丙容器的体积V < 0.5 L
C.当温度为T1 ℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1 < T2
查看答案和解析>>
科目: 来源:2016届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:填空题
(16分)(一)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)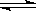 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 。(填“增大”或“减小”、“不变”)
②下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500s内N2O5的分解速率为 。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1。
(二)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ∆H < 0 (I)
NaNO3(s)+ClNO(g) K1 ∆H < 0 (I)
2NO(g)+Cl2(g) 2ClNO(g) K2 ∆H < 0 (II)
2ClNO(g) K2 ∆H < 0 (II)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=
mol,NO的转化率а1= 。其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”。
(三)已知C(s)+H2O(g)=CO(g)+H2(g)ΔH=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
查看答案和解析>>
科目: 来源:2016届吉林省长春市高三上学期期中测试化学试卷(解析版) 题型:选择题
2015年8月12日天津港瑞海公司危险化学品仓库发生特大火灾爆炸事故,事故警示我们,化学药品的安全存放是非常重要的。下列有关化学药品的存放说法不正确的是
A.液溴易挥发,应用少量的水液封并放在冷暗处保存
B.硝酸见光易分解、易挥发,应用棕色广口试剂瓶密封保存
C.金属钠遇到氧气和水均立即反应,应保存在煤油中或者液体石蜡里
D.碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com