
科目: 来源:2016届河南省高三第二次月考化学试卷(解析版) 题型:实验题
(12分)为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g,以下图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
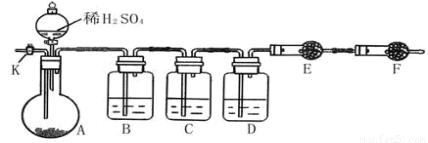
(1)将仪器连接好以后,必须进行的第一步操作是_________ ____。
(2)此实验还必须用到的最重要的仪器是 ;仪器F的作用是 。
(3)已知仪器C中装有品红溶液,其作用是________ _ ___。
(4)实验室中备有以下常用试剂:
a.浓硫酸
b.酸性高锰酸钾溶液
c.品红溶液
d.饱和碳酸氢钠溶液
e.氢氧化钠溶液
f.碱石灰
g.无水硫酸铜
h.五氧化二磷
i.无水氯化钙
①请将下列容器中应盛放的试剂序号填入相应空格:B中______,D中______,E中______。
②实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的空气。这样做的目的是 。所通空气应先经过___________试剂(填上述所供试剂的序号)处理,否则可能引起Na2SO3含量的测量结果比实际值_________(填“偏高”、“偏低”或“没影响”)。
(5)若仪器E在试验完成时增重4.4g,则Na2CO3与Na2SO3的物质的量之比为__________。
查看答案和解析>>
科目: 来源:2016届河南省高三第二次月考化学试卷(解析版) 题型:实验题
(15分)草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂,某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体的部分实验流程如下:

已知:①Ksp(CaF2)=1.46×10﹣10,Ksp(CaC2O4)=2.34×10﹣9。
②相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为0.1mol• L﹣1计算).
L﹣1计算).
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Al3+ | 3.0 | 5.0 |
Ni2+ | 6.7 | 9.5 |
(1)“粉碎”的目的是 。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图。“酸浸”的适宜温度与时间分别为 (填字母).

a.30℃、30min b.90℃、150min
c.70℃、120min d.90℃、120min
(3)证明“沉镍”工序中Ni2+已经沉淀完全的实验步骤及现象是 ,将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是 。
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为 ,第2步中加入适量NH4F溶液的作用是 。
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式: 。
(6)已知废镍催化剂中镍的质量分数为5.9%,则100kg废镍催化剂最多可制得 kg草酸镍晶体。(Ni:59,C:12,H:1,O:16)
查看答案和解析>>
科目: 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
下列实验或生产操作:①蛋白质溶液中加入硫酸铵形成沉淀;②二氧化氮经加压凝成无色液体;③石蜡催化裂化;④碘受热变成碘蒸汽;⑤照相底片被感光;⑥煤的干馏.没有新的物质生成的是
A.①④ B.②③⑥ C.①③⑤ D.①②④
查看答案和解析>>
科目: 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.1mol/L的Ca(ClO)2溶液中含ClO-数目为2NA
B.标准状况下,22.4 L三氯甲烷的原子数约为4 NA个
C.体积分别为1.0L pH==2的盐酸与硫酸溶液中氢离子数均为0.01NA
D.1 mol —OH与1 molOH-所含电子数均为9 NA
查看答案和解析>>
科目: 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍;X与Z同族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期且W不为稀有气体元素;X、Y、Z三种元素的族序数之和为16。下列说法正确的是
A.Q与W能形成10电子, 不能形成14电子、18电子分子
B.Y的最高价氧化物对应水化物的化学式只能表示为H4YO4
C.Y、Z、Q分别与X化合,只能形成AB2型化合物
D.X、Z、W中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性
查看答案和解析>>
科目: 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
下列离子方程式表达正确的是
A.漂白粉溶液中通入过量的CO2:ClO-+CO2+H2O===HClO+HCO3﹣
B.用碳酸钠溶液吸收Br2:CO32-+Br2+2H2O===Br-+BrO3-+CO2↑+4H+
C.用铜电极电解硫酸铜溶液:2Cu2++2H2O △ 2Cu↓+O2↑+4H+
D.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液,当Pb(Ac)2溶液中通入H2S时有黑色沉淀生成:Pb2++2Ac﹣+H2S===PbS+2HAc
查看答案和解析>>
科目: 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
金属钾的冶炼可采用如下方法:2KF+CaC21237~1423?CCaF2+2K↑+2C,下列有关说法合理是
A.该反应的氧化剂是KF,氧化产物是K
B.该反应能说明C的还原性大于K
C.电解KF溶液不可能制备金属钾
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
查看答案和解析>>
科目: 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:实验题
(14分)亚硝酸钠常用作食品防腐剂。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸的反应及生成气体产物的成分。
已知:①NO+NO2+2OH-===2NO2-+H2O ②气体液化的温度:NO2:21℃、NO:-152℃

(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(按左→右连接):A→C→___→______→B。
(2)组装好仪器后,接下来进行的操作是______.
(3)关闭弹簧夹K1,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体中含有NO,依据的现象是__________。
②装置B的作用是___________,装置E的作用是___________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为__________。如果没有装置C,对实验结论造成的影响是________。
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关。下列说法正确的是
A.绿色化学的核心是应用化学原理对环境污染进行治理
B.水泥、玻璃、青花瓷、水晶、玛瑙、分子筛都属于硅酸盐工业产品
C.氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理
D.通入过量的空气,可以使燃料充分燃烧,同时提高热量的利用率
查看答案和解析>>
科目: 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:选择题
对下列装置图的叙述正确的是
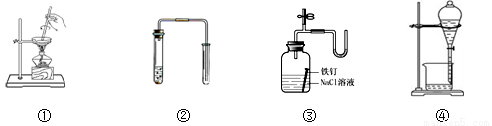
A.装置①可用于蒸发氯化镁溶液得到无水氯化镁
B.装置②可用于铜和稀硝酸制取并收集少量NO
C.装置③可用于证明铁生锈氧气参与反应
D.苯萃取碘水中的碘后,从装置④下口放出的是碘的苯溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com