
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点。右图是某同学用0.1mol•L-1KOH溶液分别滴定体积均为20mL、浓度均为0.1mol•L-1的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计).下列有关判断不正确的是
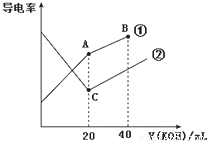
A.曲线①代表0.1 mol•L-1 KOH溶液滴定CH3COOH溶液的滴定曲线
B.在A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)═0.05 mol•L-1
C.在B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
D.在相同温度下,C点水电离的c(H+)大于A点水电离的c(H+)
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
已知:25℃时Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11下列说法正确的是
A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25℃时,Mg(OH)2固体在20 mL 0.01 mol•L-1氨水中的K比在20 mL 0.01 mol•L-1NH4Cl溶液中的Ksp小
C.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
D.25℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
一定条件下,反应:6H2+2CO2 C2H5OH+3H2O的数据如下图所示
C2H5OH+3H2O的数据如下图所示
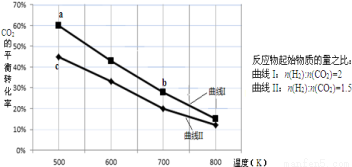
下列说法正确的是
A.该反应的△H>0
B.达平衡时,3v(H2)正=v(CO2)逆
D.b点对应的平衡常数K值大于c点
C.a点对应的H2的平衡转化率为90%
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
用下列实验装置和方法进行相应实验,能达到实验目的的是

A. 用图1所示装置分离乙醇与乙酸
B. 用图2所示装置向容量瓶中转移液体
C. 用图3所示装置制备少量氨气
D. 用图4所示装置分馏石油
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:简答题
CO2加氢合成甲醇的技术,对减少温室气体排放和减缓燃料危机具有重要意义,发生的主要反应如下:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
回答下列问题:
(1)已知:H2和CH3OH的燃烧热分别为-285.8kJ·mol-1,-726.51kJ·mol-1;以及H2O(l)=H2O(g) △H=+44kJ·mol-1;则该反应的△H=________________;
(2)该反应的平衡常数表达式为________________;
(3)在350℃时,体积为0.5L的密闭容器中,充入1molCO2和3molH2发生上述反应,测定出CH3OH的体积分数随时间变化的曲线如图所示:

①能判断该反应达到化学平衡状态的依据是__________________;
A.容器内压强不变 B.H2的体积分数不变 C.c(CH3OH)=c(H2O) D.容器内密度不变
②氢气在0~10min的平衡反应速率v(H2)=_________________________;
③在右图中标出400℃时CH3OH的体积分数随时间变化的曲线。
(4)科学家预言,燃料电池将是21世纪获得电力的重要途径,美国已计划将甲醇燃料用于军事目的。一种甲醇燃料电池是采用铂或碳化钨作电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向另一个电极通入空气。试回答下列问题:

①这种电池放电时,b处通入______________,发生的电极反应方程式是_____________________。
②若电解液中的3molH+通过质子交换膜,则消耗甲醇__________L(标准状况)。
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:实验题
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
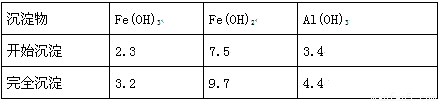
回答下列问题:
(1)加入过量废铁屑的目的是________________________(用离子方程式表示);加入少量NaHCO3的目的是________________________;该工艺中“搅拌”的作用是________________________;
(2)反应Ⅱ中的离子方程式为__________;该流程中可以循环、回收利用的物质是________;
(3)生产中碱式硫酸铁溶液蒸发时需要在减压条件下的原因是________;
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-;为检验所得产品中是否含有Fe2+,应使用的试剂为______。(填写字母)
A.酸性KMnO4溶液 B.KSCN溶液 C.氯水D.NaOH溶液
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:实验题
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱之一。下面是它的一种实验室合成路线:
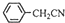 +H2O+H2SO4
+H2O+H2SO4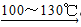
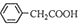 +NH4HSO4
+NH4HSO4
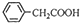 +Cu(OH)2→(
+Cu(OH)2→(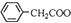 )2Cu+H2O
)2Cu+H2O
已知:苯乙腈的熔点为-23℃,不溶于水;
苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)制备苯乙酸的装置示意图如图(加热和夹持装置等略):在250mL三口瓶a中加入70mL 70%硫酸.配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是__________;
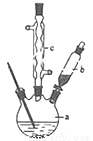
(2)将a中的溶液加热至100℃,再由b缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应.在装置中,仪器c的名称是__________;其作用是__________;
(3)反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是__________,下列仪器中可用于分离苯乙酸粗品的是__________;
A.分液漏斗 |
B.漏斗 |
C.烧杯 |
D.直形冷凝管 |
E.玻璃棒
(4)提纯苯乙酸的方法是__________,最终得到44g纯品,则苯乙酸的产率是__________;
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是__________;
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:填空题
新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,价电子的电子排布式_________________,价电子所在电子层的轨道数______;
②LiBH4由Li+和BH4-构成,BH4-的空间构型是___________,B原子的杂化轨道类型是______;
③Li、B、Cl元素的电负性由大到小排列顺序为______________;
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+________H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如下表所示:

M是_______(填元素符号);
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞边长a=480pm,Na+半径为104pm,H-的半径________pm,NaH的理论密度是_______________g•cm-3。(用NA表示)
查看答案和解析>>
科目: 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:推断题
下图为以葡萄糖为原料合成有机物X,请回答下列问题:

已知:①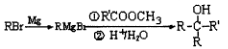
②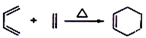
③有机物A的相对分子质量为90,9.0g A完全燃烧生成13.2gCO2和5.4gH2O,且1molA与Na反应生成1molH2、与NaHCO3反应生成1molCO2,核磁共振氢谱图中有4个吸收峰,且面积比为3:1:1:1
(1)A的分子式___________;A→B的反应类型为___________;
(2)D的结构简式___________;
(3)写出C2H6O→E转化的化学方程式___________;
(4)一定条件下A能合成一种可降解高分子材料M,写出其反应方程式___________;
(5)符合下列条件的C的同分异构体有________ 种,其中不能使溴水褪色的结构简式为___________。
①能发生水解反应 ②能发生银镜反应
查看答案和解析>>
科目: 来源:2016届安徽省高三毕业班最后一卷理综化学试卷(解析版) 题型:选择题
《天工开物》是世界第一部记录农业和手工业生产技术的百科全书,以大量生动细节留存了丰富的古代科技史料,被誉为“百科全书之祖”。下列关于书中描述的解释正确的是( )
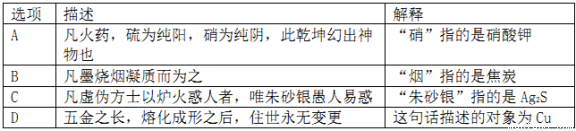
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com