
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题
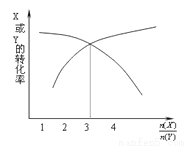
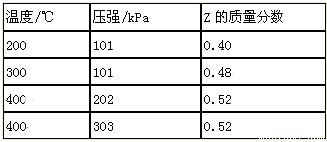
一定条件下,将X和Y两种气体按不同比例放入固定容积的密闭容器中,反应达平衡后,测得X、Y的转化率与起始时物质的量之比的关系如下图。改变温度和压强,生成物Z的百分含量见下表,则该反应的化学方程 式可表示为
式可表示为
A.3X(g)+Y(g)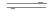 3Z(g) ΔH<0
3Z(g) ΔH<0
B.X(g)+3Y(g)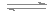 4Z(g) ΔH>0
4Z(g) ΔH>0
C.3X(g)+Y(g)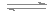 4Z(g) ΔH>0
4Z(g) ΔH>0
D.X(g)+3Y(g)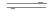 3Z(g) ΔH<0
3Z(g) ΔH<0
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题

















































 相同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)
相同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)△H=一92kJ/mol。实验测得起始、平衡时的
2NH3(g)△H=一92kJ/mol。实验测得起始、平衡时的 有关数据如下表:
有关数据如下表:
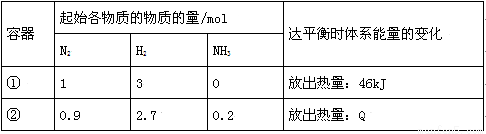
下列叙述错误的是
 A.容器①、②中反应的平衡常数
A.容器①、②中反应的平衡常数 相等
相等
 B.平衡时,两个容器中NH3的体积分数均为1/3
B.平衡时,两个容器中NH3的体积分数均为1/3
 C.容器②中达平衡时放出的热量Q=46 kJ
C.容器②中达平衡时放出的热量Q=46 kJ
 D.若容器①体积为2L,则平衡时放出的热量<46kJ
D.若容器①体积为2L,则平衡时放出的热量<46kJ
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中t2>t1):

下列说法正确的是
A.反应在t1 min内的平均速率为v(H2)= mol·L-1·min-1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60mol CO和1.20m ol H2O,到达平衡时n(CO2)=0.40mol
ol H2O,到达平衡时n(CO2)=0.40mol
C.保持其他条件不变,向平衡体系中再通入0.20mol H2O(g),△H增大
D.温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题
某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g) 2C(g)测得平衡时A、B、C物质的量之比为n(A):n(B):n(C)=1:1:2,若保持温度不变,以1:1:2的物质的量之比再充入A、B和C,下列判断中正确的是
2C(g)测得平衡时A、B、C物质的量之比为n(A):n(B):n(C)=1:1:2,若保持温度不变,以1:1:2的物质的量之比再充入A、B和C,下列判断中正确的是
A.平衡不移动
B.平衡向逆反应方向移动
C.新平衡时各物质的浓度都比原平衡时增大
D.C的质量分数减小
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题
在气相条件下(T=500 K),有相同体积的甲、乙两容器,甲容器充人1 g SO2、l gO2,乙容器充人2 g SO2、2g O2则下列叙述中正确的是
A.化学反应速率:乙>甲 B.平衡后SO2的浓度:乙<甲
C.SO2转化率:乙<甲 D.平衡后O2的体积分数:乙>甲
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题
反应N2O4(g) 2NO2(g)在温度为T1、T2(T2>T1)时,平衡体系中NO2的体积分数随压强如图所示。下列说法正确的是
2NO2(g)在温度为T1、T2(T2>T1)时,平衡体系中NO2的体积分数随压强如图所示。下列说法正确的是
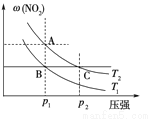
A.由图可知B点时平衡常数与C点时相同
B.A、C两点气体 的颜色:A深,C浅
的颜色:A深,C浅
C.A、C两点气体的平均相对分子质量:A<C
D.保持容器体积不变,再充入N2O4气体,N2O4的转化率增大
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:填空题
反应m A+n B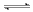 p C在某温度下达到平衡。
p C在某温度下达到平衡。
(1)若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是_______。
(2)若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向_______方向移动。(填“正反应”或”逆反应”)
(3)如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为____态。(填“固态”或“液态”或“气态”)
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:填空题
化学平衡原理在工农业生产中发挥着重要的指导作用。
(1) 反应C(s)+CO2(g) 2CO(g)平衡常数K的表达式为 ;
2CO(g)平衡常数K的表达式为 ;
已知C(s) + H2O(g)  CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)  CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为 。
CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为 。
(2)已知某温度下,反应2SO2+O2 2SO3,的平衡常数K=19 mol·L-1。在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应是否达到化学平衡状态?计算过程和结论如下 :
2SO3,的平衡常数K=19 mol·L-1。在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应是否达到化学平衡状态?计算过程和结论如下 :
(3)若未达到,反应向 (填“正反应”或“逆反应”) 方向进行。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:填空题
在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:

(1)写出该反应的平衡常数表达式:K=___________________。已知:K(300℃)> K(350℃),该反应是________热反应。
K(350℃),该反应是________热反应。
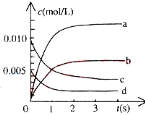
(2)右图 中表示NO2的变化的曲线是_______。用O2表示从0~2s内该反应的平均速率v=_________。
中表示NO2的变化的曲线是_______。用O2表示从0~2s内该反应的平均速率v=_________。
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO2气体 b、适当升高温度
c、增大O2的浓度 d、选择高效的催化剂
查看答案和解析>>
科目: 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:填空题
在一个容积固定为2L的密闭容器中,发生反应aA(g)+bB(g) pC(g)△H=?。反应情况记录如下表:
pC(g)△H=?。反应情况记录如下表:

请仔细分析,根据表中数据回答下列问题:
(1)a= ____________,b= _______________, p=_____________。
(2)第2min到第4min内A的平均反应速率v(A)= _________ mol•L-1•min-1。
(3)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8min时分别改变了某一反应条件,则改变的条件分别可能是:
①第2min:___________ ______或_____________;
②第6min ________________________;
③第8min _______________________ ;
(4)若从开始到第4min建立平衡时反应放出的热量为235.92kJ,则该反应的△H=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com