
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
在2A(g)+B(g) = 3C(g)+4D(g)反应中,表示该反应速率最快的是
A.vA=0.5mol·L-1·s-1 B.vB=0.3 mol·L-1·s-1
C.vC=0.8 mol·L-1·s-1 D.vD=1.0 mol·L-1·s-1
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
1000K时,反应C(s)+2H2(g)  CH4(g)的 K=8.28×107,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述平衡
CH4(g)的 K=8.28×107,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述平衡
A.向正反应方向移动 B.向逆反应方向移动
C.达到平衡 D.无法判断移动方向
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。电解质溶液为KOH溶液,电池反应为: Cd +2NiO(OH)+2H2O 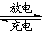 Cd(OH)2+2Ni(OH)2,下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2,下列有关镍镉电池的说法正确的是
A、充电过程是化学能转化为电能的过程
B、充电时阳极反应为Cd(OH)2+2e—== Cd + 2OH -
C、放电时电池内部OH - 向正极移动
D、充电时与直流电源正极相连的电极上发生Ni(OH)2转化为NiO(OH)的反应
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。某兴趣小组的实验数值结果大于57.3 kJ·mol-1(中和热),原因可能是
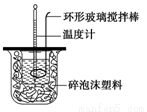
A.实验装置中小烧杯杯中低于大烧杯杯口
B.用浓硫酸代替了稀硫酸
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
下列事实能说明NH3·H2O一定是弱电解质的是
A.常温下,NH3·H2O溶液能使酚酞变红;
B.氨气极易溶于水;
C.常温下,体积、pH均相同的NH3·H2O溶液和NaOH溶液,与同浓度HCl溶液中和时,消耗HCl溶液的体积:前者>后者;
D.常温下,将pH=13的醋酸钠溶液稀释到1000倍,测得pH>10
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
下列关于反应过程中能量变化的说法正确的是
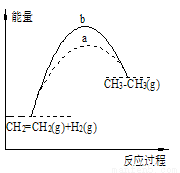
A.图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH<0使用和未使用催化剂时,反应过程中的能量变化
B.己知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2。则ΔH1>ΔH2
C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
D.在一定条件下,某可逆反应的ΔH=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
下列是有关外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达
均正确的是
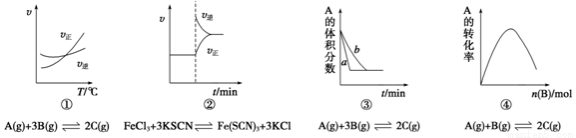
A.①是其他条件一定时,反应速率随温度变化的图像,则正反应ΔH>0
B.②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像
C.③是在有无催化剂存在条件下,建立平衡过程的图像,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率的图像
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:选择题
相同温度、相同容积的四个密闭容器中进行同样的可逆反应:
2X(g)+Y(g) 3W(g)+2Z(g) △H=-Q kJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如下表,下列说法正确的是
3W(g)+2Z(g) △H=-Q kJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如下表,下列说法正确的是
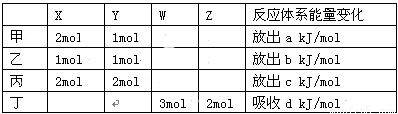
A.平衡时丙容器中Z的物质的量浓度最大
B.c+d>Q
C.平衡时,甲容器中的反应速率比丁容器中的慢
D.X的转化率为:甲<乙<丙
查看答案和解析>>
科目: 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:填空题
化学反应原理对化学反应的研究具有指导意义。
(1)机动车废气排放已成为城市大气污染的重要来源。
①气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g) △H >0。汽车启动后,气缸内温度越高,单位时间内NO排放量越大,请分析两点原因 、 。
2NO(g) △H >0。汽车启动后,气缸内温度越高,单位时间内NO排放量越大,请分析两点原因 、 。
②汽车汽油不完全燃烧时还产生CO,若设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g) ΔH>0,该设想能否实现? (选填“能”或“不能”),依据是 。
(2)氯气在298K、100kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有1/3与水反应。该反应的化学方程式为 ,在上述平衡体系中加入少量NaOH固体,溶液中Cl—浓度 (选填“增大”、“减小”或“不变”)。
(3)一定条件下,Fe3+和I—在水溶液中的反应是2I—+2Fe3+ I2+2Fe2+,当反应达到平衡后,加入CCl4充分振荡,且温度不变,上述平衡向 (选填“正反应”或“逆反应”)方向移动。请设计一种使该反应的化学平衡逆向移动的实验方案 。
I2+2Fe2+,当反应达到平衡后,加入CCl4充分振荡,且温度不变,上述平衡向 (选填“正反应”或“逆反应”)方向移动。请设计一种使该反应的化学平衡逆向移动的实验方案 。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2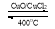 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.此条件下反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
①写出此条件下,反应A的热化学方程式 。
②断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com