
科目: 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料,又可称为燃料。工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H
CH3OH(g) △H
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2=-58kJ•mol-1
CH3OH(g)+H2O(g) △H2=-58kJ•mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:

则x=____________;
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化关系如图中状态I(图中实线)所示。图中数据A(1,6)代表在1min时H2的物质的量是6mol。
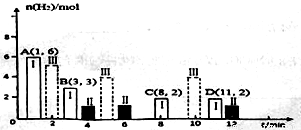
①T℃时状态I条件下,0~3min内CH3OH的平均反应速率v=_______mol/(L·min),平衡常数K=_____;
②其他条件不变时,仅改变某一条件后测得H2的物质的量随时间变化如图中状态Ⅱ所示,则改变的条件可能是_____;
③其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度_______(填“>”、“<”或“=”)T℃;
④若状态Ⅱ的平衡常数为K2,状态Ⅲ的平衡常数为K3,则K2_______(填“>”、“<”或“=”)K3;
⑤一定温度下同,此反应在恒容容器中进行,能判断该反应达到化学平衡依据的是_______。
a.容器中压强不变
b.甲醇和水蒸汽的体积比保持不变
c.v正(H2)=3v逆CH3OH)
d.2个C=O断裂的同时有6个H—H断裂
查看答案和解析>>
科目: 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:实验题
二氯化砜(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2,装置如图(有些支持装置省略了)所示。
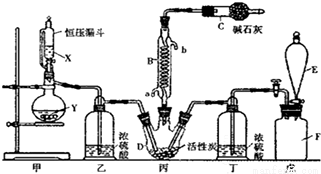
已知:SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。
(1)E中的试剂是饱和食盐水,戊是贮气装置,则F瓶中气体的实验室制法是_______(用方程式表示);
(2)B处反应管冷却水应从___________(填“a”或“b”)接口通入;
(3)装置乙和丁的作用是___________;
(4)恒压漏斗具有特殊的结构,主要目的是___________;
(5)写出二氯化砜(SO2Cl2)水解反应的方程式___________;
(6)SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸,选用下面的装置和药品探究亚硫酸与次氯酸的酸性性强弱
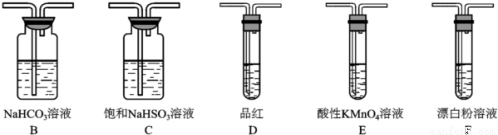
装置连接顺序为A、_____、_____、_____、D、F,其中装置C的作用是_____,通过__________________________现象即可证明亚硫酸的酸性强于次氯酸。
查看答案和解析>>
科目: 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:填空题
【化学选修2:化学与技术】硝酸铵可用作化肥、军用炸药、杀虫剂、冷冻剂等。工业制取硝酸铵的工艺流程如下:

(1)合成氨气的工业设备名称_______________,设备中设置热交换器的目的是____________,合成氨的原料气必须先脱硫,目的是_______________;
(2)吸收塔中反应的化学方程式为_________________________,从生产流程看,吸收塔中需要补充空气,其原因是_______________;
(3)生产硝酸的过程中常会产生氮的氧化物,可用如下三种方法处理:
方法一:碱性溶液吸收法
NO+NO2+2NaOH═2NaNO2+H2O;2NO2+Na2CO3═NaNO2+NaNO3+CO2
方法二:NH3还原法
8NH3(g)+6NO2(g)═7N2(g)+12H2O(g)△H=-2635kJ/mol(NO也有类似的反应)
方法三:甲烷吸收法
CH4(g)+2NO2═CO2(g)+N2+2H2O(g)△H=+867kJ/mol(NO也有类似的反应)
上述三种方法中,方法一的主要缺点是_______________;
方法三和方法二相比,方法三的缺点是_______________;
(4)工业上也可以通过电解NO制备NH4NO3,其工作原理如图所示.

①图中通入NH3的目的是_______________;
②若维持电流强度为3A,电解2小时,理论上可制得NH4NO3的最大质量为_____g;(已知F=96500C•mol-l)(保留2位有效数字).
(5)某化肥厂用NH3制备NH4NO3.己知:NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其他损耗)的百分比为______________。
查看答案和解析>>
科目: 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:填空题
【化学选修3:物质结构与性质】Ⅰ.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是__________,N2F2分子中N原子的杂化方式是_____________,1mol N2F2含有___________个σ键.
(2)高温陶瓷材料Si3N4晶体中键角N-Si-N___Si-N-Si(填“>”“<”或“=”),原因是__________;
II.金属元素在现代工业中也占据极其重要的地位,钛也被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大,是宇航、航海、化工设备等的理想材料。
(4)基态钛原子核外共有________种运动状态不相同的电子.金属钛晶胞如下图1所示,为_______堆积(填堆积方式).

(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2.化合物乙的沸点明显高于化合物甲,主要原因是_____________;化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为_____________;
(6)钙钛矿晶体的结构如图3所示.假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被________个氧离子包围。
查看答案和解析>>
科目: 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:推断题
【化学选修5:有机化学基础】A(C3H6)是基本有机化工原料,由A制备聚合物C和 的合成路线(部分反应条件略去)如图所示:
的合成路线(部分反应条件略去)如图所示:

已知:
回答下列问题:
(1)A的名称是______________,B含有的官能团的名称是(写名称)
(2)C的结构简式为______________,D→E的反应类型为______________;
(3)E→F的化学方程式为______________;
(4) 中最多有_______个原子共平面,
中最多有_______个原子共平面,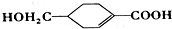 发生缩聚反应生成有机物的结构简式为______________;
发生缩聚反应生成有机物的结构简式为______________;
(5)B的同分异构体中,与B具有相同的官能团且能发生银镜反应的共有_________种;其中核磁共振氢谱为3组峰,且峰面积之比为6:1:1的是_____________(写结构简式).
(6)结合题给信息,以乙烯、HBr为起始原料制备丙酸,设计合成路线(其他试剂任选).合成路线流程图示例: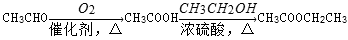
查看答案和解析>>
科目: 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:选择题
从安全的角度,下列说法正确的是
A.水银温度计不慎打破,用胶头滴管将水银吸出放入水封的瓶中,残破的温度计插入装有硫粉的广口瓶中
B.用氢气还原氧化铜的实验中,开始应该先点燃酒精灯后通氢气
C.遇到氯气泄漏时,应立即关闭氯气罐,用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
D.乘坐火车时,严禁携带白磷、汽油、氯化钠等易燃易爆物品
查看答案和解析>>
科目: 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:选择题
用下列分离装置进行相应实验,能达到相应实验目的的是( )

A.用图I除去CO2中含有的少量Cl2
B.用图Ⅱ蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图Ⅲ分离NaCl和Na2SO4的混合溶液
D.用图Ⅳ分离CCl4萃取碘水中的碘后已分层的有机层和水层
查看答案和解析>>
科目: 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑
B.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O
C.Ca(HCO3)2溶液与少量NaOH溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O
D.明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+
查看答案和解析>>
科目: 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:选择题
塑化剂(DCHP)常用于塑料加工,其中一种制备方法如下:
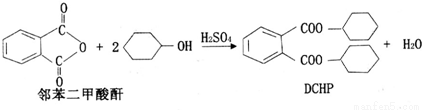
下列说法正确的是( )
A.DCHP的分子式为C20H28O4
B.上述制备DCHP的反应属于取代反应
C.DCHP苯环上的一氯代物有4种
D.1molDCHP最多可与含4molNaOH的溶液反应
查看答案和解析>>
科目: 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:选择题
全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是( )
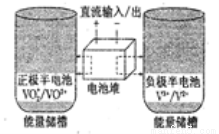
A.放电时,右槽发生还原反应
B.放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
C.充电时,每转移1mol电子,n(H+)的变化量为1mol
D.充电时,阴极电解液pH升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com