
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值。下列说法正确的是
A.1mol•L ﹣1的NaClO溶液中含有ClO﹣的数目为NA
B.常温常压下,分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
C.标准状况下,11.2 L CH3CH2OH 中含有的氢原子数目为3NA
D.室温下,1L pH=13的Ba(OH)2溶液中,OH﹣离子数目为0.2NA
pH=13的Ba(OH)2溶液中,OH﹣离子数目为0.2NA
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
能正确表示下列反应的离子反应方程式为
A.NH4HCO3稀溶液与过量的KOH稀溶液反应:NH4++HCO3﹣+2OH﹣=CO32﹣+NH3↑+2H2O
B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42﹣沉淀完全:
2Al3++3SO42﹣+3Ba2++6OH ﹣=2Al(OH)3↓+3BaSO4↓
C.向FeBr2溶液中通入足量氯气:2Fe2++4Br﹣+3Cl2=2Fe3++2Br2+6Cl﹣
D.醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
现有6.4g铜与过量硝酸(8mol/L,50mL)充分反应,硝酸的还原产物为NO和NO2,反应后溶液中含有H+ 0.05mol。( 假定反应前后溶液体积不变),下列说法不正确的是
假定反应前后溶液体积不变),下列说法不正确的是
A.NO与NO2的物质的量之比为1:5
B.反应后溶液中所含NO3﹣的物质的量浓度为0.5 mol/L
C.被还原的硝酸的物质的量为0.15 mol
D.上述过程转移电子总的物质的量为0.2 mol
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s) NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g) H2(g)+I2(g)达到平衡时,c(H2)=0.5mol•L﹣1,c(HI)=3mol•L﹣1,则此温度下反应①的平衡常数为
H2(g)+I2(g)达到平衡时,c(H2)=0.5mol•L﹣1,c(HI)=3mol•L﹣1,则此温度下反应①的平衡常数为
A.12 B.16 C.20 D.25
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
下列溶液的物质的量浓度关系正确的是( )
A.NaHCO3溶液中:c(Na+)>c(CO32﹣)>c(HCO3﹣)>c(OH﹣)
B.室温下,pH=3的盐酸与pH=11的氨水等体积混合,所得溶液中:c(Cl﹣)>c(NH4+)
C.0.1mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(CH3COO﹣)+c(OH﹣)=c(H+)+c(Na+)
D.CH3COONa溶液与CH3COOH溶液等物质的量混合后溶液呈酸性,所得溶液中:c(CH3COOH)>c(CH3COO﹣)>c(Na+)>c(H+)
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
25℃,向50mL 0.018mol/L AgNO3溶液中加入50mL 0.02mol/L 盐酸生成沉淀,已知:Ksp(AgCl)=1.8×10﹣10,则生成沉淀后的体系中c(Ag+)为( )
A.1.8×10﹣7mol/L B.1.8×10﹣8 mol/L C.1.8×10﹣9mol/L D.1.8×10﹣10mol/L
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:选择题
一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月,其电池反应为:2CH3OH+3O2+4OH﹣ 2CO32﹣+6H2O,则有关说法正确的是 ( )
2CO32﹣+6H2O,则有关说法正确的是 ( )
A.放电时CH3OH参与反应的电极为正极
B.放电时负极的电极反应为CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O
C.标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
D.放电一段时间后,通入氧气的电极附近溶液的pH降低
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:实验题
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
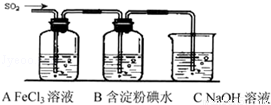
(1)SO2与Fe3+反应的还原、氧化产物分别是 、 (填离子符号)。
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3
B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧
D.铜与热浓H2SO4
(3)装置C的作用是 。
(4)如果有280mL SO2气体(已折算为标态)进入C装置中,则C中,50mL NaOH溶液的浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
 方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I﹣的还原性弱于SO2的现象是 ,写出有关离子方程式: 。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:实验题
锰的用途非常广泛,以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1. | 5.0×10-22 | 1.0×10-22 |
(1)步骤Ⅰ中,为加快溶浸速率,可采取的措施是: 。
(2)步骤Ⅱ中,须加氨水调节溶液的pH为5.0~6.0,则滤渣1的主要成分为 (填化学式)。已知MnO2的作用为氧化剂,则得到该滤渣1所涉及的离子方程式为 、 。
(3)步骤Ⅲ中,所加(NH4)2S的浓度不宜过大的原因是 。
(4)滤液2中,c(Co2+):c(Ni2+)= 。
(5)将质量为akg的碳酸锰矿经上述流程处理后得到单质Mn b kg。若每一步都进行完全,滤渣1为纯净物,质量为c kg,则原碳酸锰矿中MnCO3的质量分数为  。(用含a、b、c的式子表达,无需化简)
。(用含a、b、c的式子表达,无需化简)
查看答案和解析>>
科目: 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:简答题
氮及其化合物在工业生产和国防建设中有广泛应用。回答下列 问题:
问题:
(1)氮气性质稳定,可用作保护气。请用电子式表示氮气的形成过程: 。
(2)联氨(N2H4)是一种还原剂。已知:H2O(l)=H2O(g)△H=+44kJ/mol。试结合下表数据,写出N2H4 (g)燃烧热的热化学方程式: 。
化学键 | N—H | N—N | N=N | N≡N | O=O | O—H |
键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
(3)KCN可用于溶解难溶金属卤化物。将Ag I溶于KCN溶液中,形成稳定的Ag(CN)2-,该转化的离子方程式为: 。若已知Ksp(AgI)=1.5×10-16,K稳Ag(CN)2-]=1.0×1021,则上述转化方程式的平衡常数K= 。(提示:K稳越大,表示该化合物越稳定)
I溶于KCN溶液中,形成稳定的Ag(CN)2-,该转化的离子方程式为: 。若已知Ksp(AgI)=1.5×10-16,K稳Ag(CN)2-]=1.0×1021,则上述转化方程式的平衡常数K= 。(提示:K稳越大,表示该化合物越稳定)
(4)氨的催化氧化用于工业生产硝酸。该反应可设计成新型电池,试写出碱性环境下,该电池的负极电极反应式: 。
(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2 N2O4其相关图像如下。
N2O4其相关图像如下。
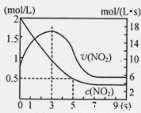
①0~3s时v(NO2)增大的原因是 。
②5s时NO2转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com