
科目: 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:简答题
随着化石能源的大量开采以及污染的加剧,污染气体的治理和开发利用日益迫切。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成;
SO2(g) + I2(g) + 2H2O(g) = 2HI(g) + H2SO4(l) ∆H=a kJ/mol ①
2H2SO4(l) = 2H2O(g) + 2SO2(g) + O2(g) ∆H= b kJ/mol ②
2HI(g) = H2(g) + I2(g) ∆H= c kJ/mol ③
则2H2O(g) = 2H2(g) + O2(g) ∆H= kJ/mol
(2)CO2 和CH4 是两种重要的温室气体,以表面覆盖有Cu2Al2O4 的二氧化钛为催化剂。可以将CO2 和CH4直接转化为乙酸。
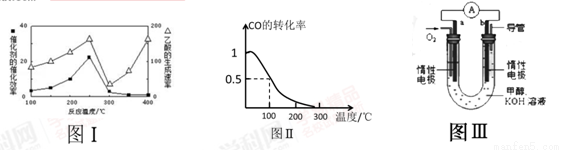
①不同温度下催化剂的催化效率与乙酸的生成速率如图Ⅰ所示,该反应体系应将温度控制在 ℃左右。
②将Cu2Al2O4 溶解在稀硝酸中的离子方程式为 。
(3)甲醇(CH3OH)被称为21世纪的新型燃料。在体积为V L的某反应容器中,a mol CO与2a mol H2 在催化剂作用下反应生成甲醇:CO(g) + 2H2(g)  CH3OH(g) ,CO的平衡转化率与温度的关系如图Ⅱ所示:
CH3OH(g) ,CO的平衡转化率与温度的关系如图Ⅱ所示:
①该反应是 (填“放热”或“吸热”)反应
②在其他条件不变的情况下,反应容器中再增加amol CO与2amolH2 ,达到新平衡时,CO的转化率 (填“增大”、“减小”或“不变”)。
③100℃,反应CH3OH(g)  CO(g) + 2H2(g) 的平衡常数为 (用含有a、V的代数表示)。
CO(g) + 2H2(g) 的平衡常数为 (用含有a、V的代数表示)。
(4)某实验小组设计了如图III所示的甲醇燃料电池装置。
①该电池工作时,OH- 向 (填“a”或“b”)极移动
②工作一段时间后,测得该溶液的pH减小,该电池负极反应的电极反应式为: 。
查看答案和解析>>
科目: 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:实验题
以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:
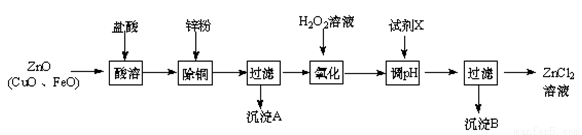
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
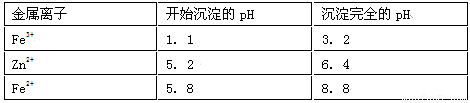
(1)加入H2O2溶液发生反应的离子方程式为 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 (选填序号:a.ZnO;b.Zn(OH)2 ;c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 。
(3)氯化锌能催化乳酸(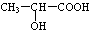 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ;阴极的电极反应为 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 。
查看答案和解析>>
科目: 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:实验题
(化学与技术)聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·xH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:
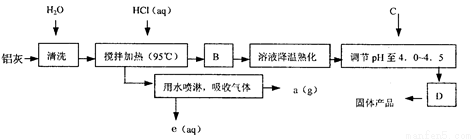
 (1)搅拌加热操作过程中发生反应的离子方程式 ;
(1)搅拌加热操作过程中发生反应的离子方程式 ;
(2)生产过程中操作B和D的名称均为 (B和D为简单操作)。
(3)反应中副产品a是 (用化学式表示)。
(4)生产过程中可循环使用的物质是 (用化学式表示)。
(5)调节pH至4.0~4.5的目的是 。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程中C物质可选用 。
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2
查看答案和解析>>
科目: 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:填空题
(物质结构与性质)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
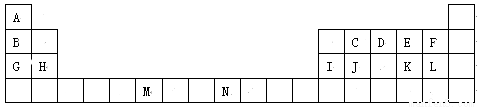
试回答下列问题:
(1)请写出元素N的基态原子电子排布式 。
(2)元素B、G形成的单质熔点更高的是_ ___(填化学式),原因是____ _
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是__________(填“极性”或“非极性”)分子。
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。
(5)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为 。
查看答案和解析>>
科目: 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:推断题
(有机化学基础)咖啡酸苯乙酯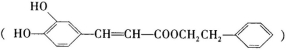 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化:
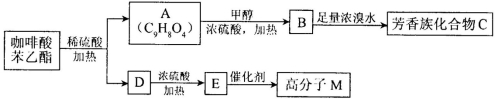
请填写下列空白。
(1)咖啡酸苯乙酯中的含氧官能团是 ;
(2)B→C发生的反应类型有 ;
(3)M的结构简式是 ;
(4)写出A→B反应的化学方程式: ;
(5)写出有机物A通过加聚反应形成高分子化合物的化学方程式 ;
(6)A的同分异构体很多种,其中,同时符合下列条件的同分异构体有 种。
①苯环上只有两个取代基;
②能发生银镜反应;
③能与碳酸氢钠溶液反应;
④能与氯化铁溶液发生显色反应。
(7)有机物H是A的一种同分异构体,且与A具有相同种类和数目的官能团,H分子中共有6种不同化学环境的氢原子,且核磁共振氢谱的峰面积比为1:1:1:1:2:2,写出满足以上条件的H的结构简式 (写出一种即可)
查看答案和解析>>
科目: 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关.下列叙述正确的是
A.煤的干馏与石油的分馏均属于化学变化
B.BaSO4在医学上用作钡餐,Ba2+对人体无毒
C.14C可用于文物的年代鉴定, 14C与 13C互为同素异形体
D.葡萄糖注射液不能产生丁达尔现象,不属于胶体
查看答案和解析>>
科目: 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1.8 g重水(D2O)中含NA个中子
B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA
C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA
D.足量的铜与含2 mol H2SO4的浓硫酸充分反应,可生成NA个SO2分子
查看答案和解析>>
科目: 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
如图是制取和收集某气体的实验装置,可用于
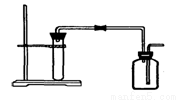
A.用Zn粒与稀HCl反应制H2
B.用大理石与稀HCl反应制CO2
C.用Cu与稀HNO3反应制NO
D.用MnO2与浓HCl反应制Cl2
查看答案和解析>>
科目: 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
常温离子液体(Ionic Liquid)也称常温熔融盐。硝酸乙基铵〔(C2H5NH3)NO3〕是人类发现的第一种常温离子液体,其熔点为12℃,已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是
A.可用作电池的电解质 B.水溶液呈碱性
C.是共价化合物 D.结构和性质类似于硝酸乙酯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com