
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
下列对第ⅣA族元素及其化合物的性质的推断一定不正确的是
A.与同族硅元素类似,锗、锡、铅都可用做半导体材料
B.锗与盐酸可能不反应,锡、铅能与盐酸反应
C.锗、锡、铅的+4价氢氧化物的碱性由弱到强的顺序为:Ge(OH)4<Sn(OH)4<Pb(OH)4
D.锗、锡、铅的金属性依次减弱
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
3.0gFe2O3和A12O3组成的混合物全部溶于200mLpH=0的硫酸,反应后向所得溶液中加入100mLNaOH溶液,恰好使Fe3+、A13+完全沉淀,则加入的NaOH的浓度c(NaOH)为
A.1mol/L
B.2mol/L
C.4mol/L
D.8mol/L
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:推断题
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属单质在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)X在周期表中的位置:____________,UW2的电子式为____________;
(2)写出下列反应的化学方程式,Z在高温下与水反应_______________________________________;
(3)U、V、W形成的10电子氢化物中,氢化物的稳定性从强到弱的顺序是____________(写化学式),V元素的氢化物极易溶于水的主要原因是__________________________,该氢化物与空气可以构成一种环保燃料电池,电解质溶液是KOH,其负极的电极反应式为____________。
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:填空题
某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,该废水的处理流程如下:

(1)过程Ⅰ:加NaOH溶液,其作用用离子方程式表示为____________,调节pH至9后,升温至30℃,通空气将氨赶出并回收;
(2)过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

①第一步反应的热化学方程式是____________;
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是____________;
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32gCH3OH转移6mol电子,则该反应的化学方程式是____________。
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:填空题
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g)ΔH>0,已知该反应在2404℃时,平衡常数K=64×10-4。
2NO(g)ΔH>0,已知该反应在2404℃时,平衡常数K=64×10-4。
请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率________;
(2)假设该反应是在恒容条件下进行,判断该反应达到平衡的标志________;
A.容器内气体压强不再变化
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.2v(N2)正=v(NO)逆
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是________(填字母序号);
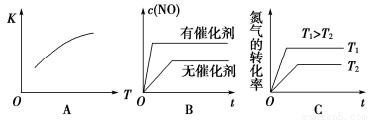
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数______;(填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应v正________v逆(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:填空题
有一混合物水溶液,含有以下离子中的若干种:Na+、NH4+、Cl—、Ba2+、HCO3—、SO42—,现各取100mL溶液分别进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液,加热,收集到标准状况下的气体448mL
③第三份加足量Ba(OH)2溶液,得沉淀4.30g,再用足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-:____________;(填“是”或“否”)
(2)由第二份进行的实验可知混合物中应含有____________离子,其物质的量浓度为____________;
(3)由第三份进行的实验可知4.30g沉淀的成份为____________,写出生成该沉淀的离子方程式:____________;
(4)溶液中肯定存在的离子是____________。
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:实验题
现有一份含有FeCl3和FeCl2固体的混合物,为测定FeCl2的含量,进行如下实验:
①称取混合物样品的质量7.06g,将样品溶解
②向溶解后的溶液中,加入足量的双氧水
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4.00g
根据实验回答下列问题:
(1)样品溶解过程中需加入___________,以防止__________________;
(2)写出溶解后的溶液与双氧水反应的离子方程式____________;
(3)过滤操作中除用漏斗外,还需要的玻璃仪器有____________;
(4)简述检验实验步骤④中沉淀已经洗涤干净的方法____________;
(5)通过实验所得数据,计算固体样品中FeCl2的质量分数:____________;
(6)实验室采用下列装置制取少量无水FeCl3固体。(已知FeCl3固体易潮解,部分夹持仪器已略去。)
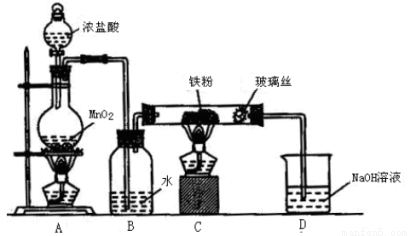
该装置存在明显缺陷,得不到无水FeCl3固体,请你对该装置进行合理的改进:____________。
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
已知:2R—Cl+2Na→R—R+2NaCl(R代表烃基),下列有机物通过上述反应可制得对二甲基环己烷的是
A.2,3—二氯丁烷
B.1,3—二氯丁烷
C.2—氯丁烷
D.2,5—二氯己烷和1,2—二氯乙烷
查看答案和解析>>
科目: 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:推断题
现设计如下路线合成有机物E(C6H8O4),(其中A的相对分子质量是56,B的相对分子质量是125)。

(1)烃A的分子式是,D的结构简式为______________;
(2)③的反应类型是____________反应;
(3)已知E为顺式结构,则其结构简式是____________;
(4)下列说法正确的是____________(填序号)
a.反应①属于加成反应
b.B与二氯甲烷互为同系物
c.C存在立体异构体
d.D能使溴水褪色
(5)若C转化为D经过如下4步反应完成: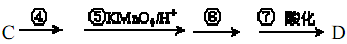 。
。
则④的化学方程式是____________,⑥所需的无机试剂及反应条件是____________。
查看答案和解析>>
科目: 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关,对下列现象或事实的解释正确的是
选项 | 现象或事实 | 解释 |
A | 用热的烧碱溶液洗去油污 | Na2CO3可直接与油污反应 |
B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
C | 施肥时,草木灰(有效成分为K2CO3 )不能与NH4Cl 混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com