
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无 “0”刻度,滴定管有“0”刻度
“0”刻度,滴定管有“0”刻度
B.如果酒精刚刚着火,可直接用湿抹布盖灭;若酒精燃烧有一定时间,则用CO2灭火器灭火
C.室温下,浓度均为0.1mol•L-1Na2S2O3和H2SO4溶液,分别取5mL与10mL混合,10mL与10mL混合,可验证Na2S2O3浓度对反应速率的影响
D.往K2CrO4溶液中滴加稀硫酸,溶液由黄色变为橙色
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列有关钢铁腐蚀和防护的说法不正确的是( )
A.自行车的钢圈上镀一层铬,防止生锈
B.外加直流电源保护钢闸门时,钢闸门与电源的负极相连
C.钢铁发生吸氧腐蚀的正极反应:2H2O+O2 - 4e-===4OH-
D.钢铁发生析氢腐蚀的负极反应:Fe-2e-===Fe2+
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
瑞典ASES公司设计的曾用于驱动潜艇的液氨—液氧燃料电池示意图如图所示,下列有关说法正确的是( )

A.电极2发生氧化反应
B.电池工作时,Na+向负极移动
C.电流由电极1经外电路流向电极2
D.电极1发生的电极反应为2NH3+6OH--6e-===N2↑+6H2O
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案:将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6 mol.L-1 NaOH溶液中,当石墨棒上不再有气泡产生时,取出铁片,用水冲洗、烘干后称量,质量为m2。下列说法正确的是( )
A.设锌镀层厚度为h,锌的密度为ρ,则h=(m1-m2)/( ρS)
B.锌电极的电极反应式为 2H2O + 2e- = H2 + 2OH-
H2 + 2OH-
C.锌和石墨在碱溶液中形成原电池,外电路中电流从锌流向石墨
D.当石墨上不再有气泡时,立即取出铁皮,冲洗后用酒精灯加热烘干,铁片可能部分被氧化导致实验结果偏低
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法正确的是( )
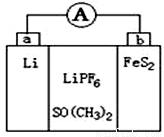
A.Li发生氧化反应,a极为阴极
B.电子由a极流出通过电流表流入b极,然后再由b极经内电 路回到a极
C.可以用水代替SO(CH3)2做溶剂
D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行可逆反应:X(g)+Y(g)  Z(g)+W(s) ΔH>0。下列叙述正确的是( )
Z(g)+W(s) ΔH>0。下列叙述正确的是( )
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.平衡后加入X,上述反应的ΔH增大
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)  cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )
cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )

A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
往2 L密闭容器中充入NO2,在三种不同条件下发生反应:2NO2(g) 2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。下列说法正确的是( )
2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。下列说法正确的是( )

A.实验2比实验1的反应容器内压强小
B.实验2比实验1使用了效率更高的催化剂
C.实验 1比实验3的平衡常数大
1比实验3的平衡常数大
D.由实验2和实验3可判断该反应是放热反应
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列关于化学实验的说法正确的是( )
A.分离物质的量之比为1:6的氯化钠和硝酸钾混合物时,可先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得到硝酸钾晶体;将母液加热蒸干得到氯化钠晶体。
B.在“反应热的测量和计算”实验时须先将用于实验的等体积等物质的量的稀NaOH和稀HCl溶液置于相同温度(一般为25℃)下保温一段时间后再混合
C.在电化学实验中常使用碳电极,实验室一般采用多孔碳棒作为碳电极。有些电化学反应中的气体产物可以自由填充在多孔碳棒的疏松空隙中,从而增大气体的吸收量。
D.为了降低HNO3与Cu反应制备NO2的速率,可以用稀硝酸代替浓硝酸
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
在容积不变的密闭容器中进行反应: 2SO2(g)+O2(g) 2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应
2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应 的影响,其中分析正确的是( )
的影响,其中分析正确的是( )
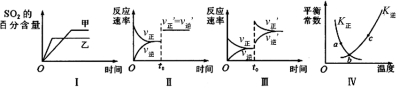
A.图I表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com