
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
在下列装置中,MSO4和NSO4是两种常见金属 的易溶盐。当K闭合时,SO从右到左通过交换膜移向M极,下列分析正确的是( )
的易溶盐。当K闭合时,SO从右到左通过交换膜移向M极,下列分析正确的是( )
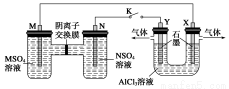
A.溶液中c(M2+)减小
B.N的电极反应式:N-2e-===N2+
C.X电极上有H2产生,发生还原反应
D.反应过程中Y电极周围生成白色胶状沉淀
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是( )

A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
已知:锂离子电池的总反应为LixC+Li1-xCoO2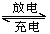 C+LiCoO2,锂硫电池的总反应为2Li+S
C+LiCoO2,锂硫电池的总反应为2Li+S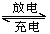 Li2S,有关上述两种电池说法正确的是( )
Li2S,有关上述两种电池说法正确的是( )
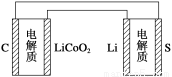
A.锂离子电池放电时,Li+向负极迁移
B.锂硫电池充电时,锂电极发生氧化反应
C.理论上两种电池的比能量相同
D.下图表示用锂硫电池给锂离子电池充电
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图,下列说法正确的是( )

A.A为电源负极
B.阳极区溶液中发生的氧化还原反应为Cr2O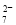 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H213.44L(标准状况)时,有0.2molCr2O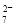 被还原
被还原
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
用惰性电极电解V L ASO4的水溶液,当阴极上有m g 金属析出(阴极上无气体产生)时,阳极上产生x L气体(标准状况),同时溶液的氢离子的浓度增加了10-2 mol·L-1 (设电解前后溶液体积不变)。则A的相对原子质量的表示式为( )
① ②
②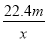 ③
③ ④
④
A.①④ B.②④ C.③④ D.①②
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
100 mL KNO3和Cu(NO3)2的混合溶液中c(NO3—)=6.0 mol/L,用石墨作电极电解此溶液,通电一段时间后,两极均收集到4. 48 L气体(标准状况),假定电解后溶液体积仍为100 mL,下列说法不正确的是( )
48 L气体(标准状况),假定电解后溶液体积仍为100 mL,下列说法不正确的是( )
A.原混合溶液中c(K+)=2mol/L
B.上述电解过程中一共转移电子0.8 mol
C.电解得到的铜的物质的量为0.2 mol
D.电解后溶液中c(H+)=2 mol/L
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
某充电电池的原理如下图所示,溶液中c(H+)=2.0 mol·L-1,阴离子为SO42-,a、b均为惰性电极,充电时右槽溶液颜色由绿色(V 3+)变为紫色(V2+)。下列对此电池叙述正确的是( )

A.充电时,b极接直流电源正极,a极接直流电源负极
B.放电过程中,左槽溶液颜色由黄色变为蓝色
C.充电过程中,a极的反应式为:VO2++2H++e—= VO2+ +H2O
D.放电时,当转移1.0 mol电子时生成1.0 mol H+且H+从左槽迁移进右槽
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:推断题
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)g在周期表中的位置是________。
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:________>________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:________。
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:________。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有 10 mL 1 mol·L-1R溶液的烧杯中滴加1 mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
10 mL 1 mol·L-1R溶液的烧杯中滴加1 mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

①写出m点反应的离子方程式:________。
②若在R溶液中改加20 mL 1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________mol。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:推断题
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,B元素的最高正价和最低负价之和为2。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)C、D、F三种元素形成的简单离子的半径由大到小的顺序是 (用离子符号表示)。
(2)由A、B两种元素以原子个数比5∶1形成离子化合物X,X的电子式为 。
(3)由A、B元素形成的化合物B2A4可以与O2、KOH溶液形成原电池,用该原电池提供的能量电解足量的CuSO4溶液,当消耗0.2mol B2A4时,若要使电解槽中溶液恢复到电解前的情况,需要向其中加入多少克什么物质?( 填质量和化学式) 。
填质量和化学式) 。
(4)A 和B 形成的某种氯化物BA2Cl 可作杀菌剂,其原理为BA2Cl 遇水反应生成一种具有强氧化性的含氧酸,写出BA2Cl 与水反应的化学方程式:__ _ 。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:填空题
甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景。
(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH =-44.0 kJ/mol
请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为________
(2)某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置。

①工作一段时间后,测得溶液的pH 。(填“增大”“减小”“不变”)
②该电池负极的电极反应为 。
(3)某金属的相对原子质量为52.00,用上述电池电解该金属的一种含氧酸盐的酸性水溶液时,阳极每放出3 360 mL(标准状况)氧气,阴极析出金属10.4 g,在该含氧酸盐中金属的化合价为 ,
在该实验中,若不考虑能量的损失,电池中消耗甲醇的质量最少是 g(结果精确至0.1 g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com