
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:选择题
25 ℃时,向 10 mL 0.01 mol·L-1KOH 溶液中滴加0.01 mol·L-1苯酚溶液,混合溶液中粒子浓度关系正确的是( )
A.当pH>7 时,c(C6H5O-)>c(K+)>c(H+)>c(OH-)
B.当pH<7 时,c(K+)> c(C6H5O-)>c(H+)>c(OH-)
C.V[C6H5OH(aq)]=10 mL 时,c(K+)=c(C6H5O-)>c(OH-)=c(H+)
D.V[C6H5OH (aq)]=20 mL 时,c(C6H5O-)+c(C6H5OH)=2c(K+)
查看答案和解析>>
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:实验题
实验室采用简易装置模拟演示工业炼铁原理,实验装置图和实验步骤如下:
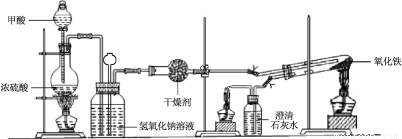

① 按上图连接好装置,检查装置气密性。
② 称取适量 Fe2O3于石英试管中,点燃Ⅰ处酒精灯,缓慢滴入甲酸。
③ 在完成某项操作后,点燃另外两处酒精灯。
④ 30 min后熄灭酒精灯,关闭弹簧夹。
⑤ 待产物冷却至室温后,收集产物。
⑥ 采用如上方法分别收集带金属网罩酒精灯(金属网罩可以集中火焰、提高温度)和酒精喷灯加热的产物。
请回答下列问题:
(1)制备CO的原理是利用甲酸(HCOOH)在浓硫酸加热条件下的分解制得,盛放甲酸的仪器名称为 ,该反应的化学方程式 。
(2)实验步骤③某项操作是指 。
(3)实验步骤④熄灭酒精灯的顺序为______________。(填I,II,III)
(4)通过查资料获取如下信息:
I.酒精灯平均温度为600℃;加网罩酒精灯平均温度为700℃,酒精喷灯平均温度为930℃。
II.资料指出当反应温度高于710℃,Fe能稳定存在,680℃~710℃之间,FeO稳定存在,低于680℃,则主要是Fe3O4。试分析酒精灯加热条件下生成Fe的原因是 。
(5)已知FeO、Fe2O3、Fe3O4氧元素的质量分数分别为:22.2%、30%、27.6%。利用仪器分析测出3种样品所含元素种类和各元素的质量分数如下表:
加热方式 | 产物元素组成 | 各元素的质量分数%[§科§网] | |
Fe | O | ||
酒精灯 | Fe和O | 74.50 | 25.50 |
带网罩酒精灯 | Fe和O | 76.48 | 23.52 |
酒精喷灯 | Fe | 100.00 | 0.00 |
分析各元素的质量分数可知前二种加热方式得到的产物为混合物,其中酒精灯加热所得产物的组成最多有_______种可能。
(6)通过进一步的仪器分析测出前二种加热方式得到的固体粉末成分均为Fe3O4和Fe,用酒精喷灯加热得到的固体粉末成分为Fe。请计算利用酒精灯加热方式混合物中Fe3O4和Fe的质量比为_____。(要求保留整数)
查看答案和解析>>
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸浆漂白和鱼药的制造。制备亚氯酸钠的工艺流程如下:

(1)要加快步骤①的反应速率,可采取的措施为 。(写一种即可)
(2)步骤①的离子方程式为 ,每生成标准状况下22.4L的ClO2,转移电子数为 。
(3)步骤②中H2O2的作用是 ;从“反应混合液”到“产品”的过程中先需蒸发溶剂,写出蒸发所需的硅酸盐仪器的名称 。
(4)NaClO2产品中通常混有少量NaCl。取样品wg,测得Na的物质的量为nmol,则该样品中NaClO2的物质的量为______mol。
查看答案和解析>>
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:填空题
氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用。
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H= 。(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3 L的恒容密闭容器中,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如下表所示:
温度(K) | 平衡时NH3的物质的量(mol) |
T1 | 2.4 |
T2 | 2.0 |
已知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
①则T1 T2(填“>”、“<”或“=”)。
②在T2 K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)= ,平衡时N2的转化率α(N2)= 。
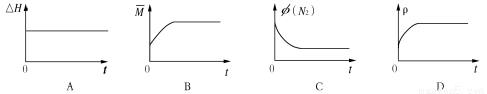
③下列图像分别代表焓变(△H)、混合气体平均相对分子质量( )、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 。
)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 。
(3)某N2H4(肼或联氨)燃料电池(产生稳定、无污染的物质)原理如图1所示。
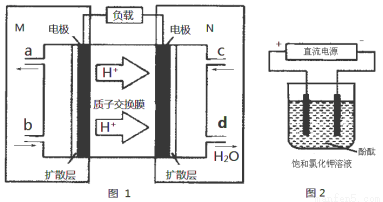
①M区发生的电极反应式为 。
②用上述电池做电源,用图2装置电解饱和氯化钾溶液(电极均为惰性电极),设饱和氯化钾溶液体积为500mL,当溶液的pH值变为13时(在常温下测定) ,若该燃料电池的能量利用率为80%,则需消耗N2H4的质量为 g(假设溶液电解前后体积不变)。
,若该燃料电池的能量利用率为80%,则需消耗N2H4的质量为 g(假设溶液电解前后体积不变)。
查看答案和解析>>
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:实验题
【化学–选修2:化学与技术】工业上设计将VOSO4中的K2S O4、SiO2杂质除去并回收得到V2O5的流程如下:
O4、SiO2杂质除去并回收得到V2O5的流程如下:

请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),操作I的名称 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+2nHA(有机层) 2RAn(有机层)+nH2SO4 (水层)
2RAn(有机层)+nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)④的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 。
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有 和 。
查看答案和解析>>
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大。A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族。回答下列问题:
(1)A、B、C第一电离能由大到小的顺序为: (用元素符号表示)。
(2)B与C形成的二元化合物中,属于非极性分子的是: (填化学式);该分子中心原子的杂化类型为: 。
(3)A、C元素形成的常见含氧酸中,分子的中心原子的价层电子对数为4的酸是 ;(填化学式,下同)酸根呈平面三角形的酸是 。
(4)E和F形成的一种化合物的晶体结构如图所示,则该化合物的化学式为 ;F的配位数为 。
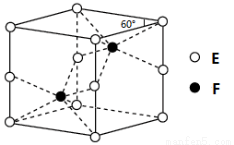
(5)D的离子可以形成多种配合物,由Dn+、Br-、C的
最高价含氧酸根和A的简单氢化物形成的1:1:1:5的某
配合物,向该配合物的溶液中滴加AgNO3溶液产生
淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物的化学式为: ;n值为 ;Dn+的基态电子排布式为: 。
查看答案和解析>>
科目: 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:实验题
【化学—选修5:有机化学基础】盐酸普鲁卡因(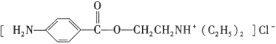 )是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
)是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
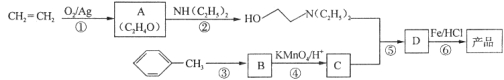
已知:①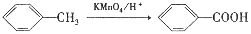
②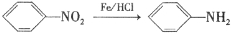
③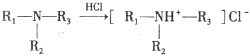
请回答以下问题:
(1)A的核磁共振氢 谱只有一个峰,则A的结构简式为____________________。
谱只有一个峰,则A的结构简式为____________________。
(2)C的结构简式为__ ________,C中含有的含氧官能团的名称为__________。
________,C中含有的含氧官能团的名称为__________。
(3)合成路线中属于氧化反应的有_________(填序号),反应③ 的反应类型为
的反应类型为 _______________。
_______________。
(4)反应⑤的化学反应方程式为______________________________________________。
(5)B的某种同系物E,相对分子质量比B大28,其中—NO2与苯环直接相连,则E的结构简式为____________________(任写一种)。
(6)符合下列条件的E的同分异构体的数目有__________种。
①结构中含有一个“—NH2”与一个“—COOH” ②苯环上有三个各不相同的取代基
(7)苯丙氨酸(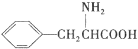 )是人体必需的氨基酸之一,写出其发生缩聚反应的化学方程式____________________________________________________________。
)是人体必需的氨基酸之一,写出其发生缩聚反应的化学方程式____________________________________________________________。
查看答案和解析>>
科目: 来源:2016届福建厦门外国语学校高三5月月考理综化学试卷(解析版) 题型:选择题
晚唐诗人李商隐的《无题·相见时难别亦难》中写到“春蚕到死丝方尽,蜡炬成灰泪始干”,下列说法正确的是
A.蚕丝属于纤维素
B.蜡烛的主要成分是石蜡,属于混合物
C.“泪”是指石蜡燃烧生成的水
D.蚕丝和石蜡完全燃烧所得产物相同
查看答案和解析>>
科目: 来源:2016届福建厦门外国语学校高三5月月考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.NA个Fe(OH)3胶体粒子的质量为107g
B.标准状况下,1L液态水中含有的H+数目为10-7NA
C.14g分子式为CnH2n的链烃中含有的碳碳双键的数目为NA/n
D.1 mol冰醋酸和l mo1乙醇经酯化反应可生成H2O分子数为NA
查看答案和解析>>
科目: 来源:2016届福建厦门外国语学校高三5月月考理综化学试卷(解析版) 题型:选择题
某有机物的结构简式如图所示,下列有关该有机物的说法正确的是
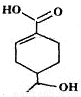
A.分子中含有四种官能团
B.1mol该有机物完全燃烧消耗O2的物质的量为10mol
C.能发生加成、取代、消去、水解等反应
D.相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生气体的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com