
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:选择题
常温,向一定体积V mL浓度均为 0.1 mol·L-1 FeCl3和FeCl2溶液中滴加NaOH溶液至pH=4,溶液中有沉淀生成,过滤,得到沉淀和滤液。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16。下列说法正确的是
A.滤液中c(Fe3+)=4.0×10-29 mol·L-1
B.沉淀为Fe(OH)3和Fe(OH)2的混合物
C.向滤液中加入少量FeCl2溶液,一定有沉淀生成
D.向滤液中继续加入NaOH溶液使pH﹥7时,一定有Fe(OH)2沉淀生成
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:选择题
用石墨作电极电解200mL一定浓度的CuSO4溶液,一段时间后停止电解,然后向电解后的溶液中加入0.1mol Cu2(OH)2CO3,可使溶液完全恢复至电解前的浓度和体积,则电解过程中电路通过电子的物质的量是
A.0.4 mol B.0.6 mol C.0.8 mol D.1.0 mol
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
常温下,某水溶液M中存在的离子有Na+、A-、H+、OH-。根据题意回答下列问题:
(1)若溶液M由0.1 mol·L-1的HA溶液与0.1 mol·L-1的NaOH溶液等体积混合而得,则溶液M的pH不可能________7(填“>”、“<”或“=”)。
(2)若溶液M的pH>7,则c(Na+)________c(A-)(填“>”、“<”或“=”)。
(3)常温下,若溶液M由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,则下列说法中正确的是________(填字母)。
A.若溶液M呈中性,则溶液M中c(H+)+c(OH-)=2×10-7 mol·L-1
B.若V1=V2,则溶液M的pH一定等于7
C.若溶液M呈酸性,则V1一定大于V2
D.若溶液M呈碱性,则V1一定小于V2
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
(1)25℃时,在等体积的 ① pH=0的H2SO4溶液、② 0.05 mol/L的Ba (OH)2溶液、③ pH=10的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比 。
(2)常温下,0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后:
c(CH3COO?) + c(CH3COOH)= mol/L
c(H+) c(CH3COO?) - c(CH3COOH) +2c(OH?) (填“>”、“<”或“=”)
(3)常温下,把pH=11的氢氧化钠溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系是 。
(4)常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,混和液pH=7。则两溶液的体积比是 。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
在2 L的密闭容器内,800℃时反应2NO(g)+O2(g)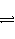

 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=_____________________。已知:K300℃>K350℃,则该反应是______热反应。
(2)右图表示NO2的变化的曲线是_______。用O2表示从0~2 s内该反应的平均速率v=_______________。
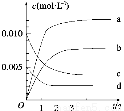
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO、OH- |
在下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
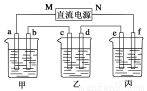
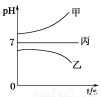
接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16 g。常温下各烧杯中溶液的pH与电解时间t的关系如上图。据此回答下列问题:
(1)M为电源的_____极(填“正”或“负”),电极b上发生的电极反应为__________________。
(2)电极e上生成的气体在标准状态下的体积为________。
(3)写出乙烧杯中的电解池反应_______________________。
(4)要使丙烧杯中的C溶液恢复到原来的状态,正确的操作__________(计算出相关数据)。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
一种将电解池与燃料电池相组合的新工艺可使氯碱工业节能30%以上。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
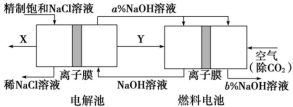
(1)图中X、Y分别是_______、______(填化学式),a ___b(填“>”、“<”或“=”)。
(2)燃料电池中负极的电极反应式是______________________。
(3)电解池中总反应的离子方程式是__________________________。
(4)假设该装置的能量利用率可达70%,要电解制得2.4 mol NaOH,燃料电池需消耗标准状况下的空气________L。(空气中O2的体积分数为20%)
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:实验题
“烂版液”是制印刷锌版时,用稀硝酸腐蚀锌版后得到的“废液”(含有少量的Cl-、Fe3+)。某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:
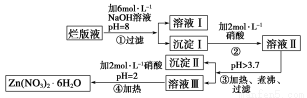
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是______(填化学式,下同)。
(2)沉淀Ⅰ的主要成分是____________。
(3)操作③中加热煮沸的目的是_____________;此步操作的理论依据是_______________。
(4)操作④保持pH=2的目的是____________。
查看答案和解析>>
科目: 来源:2015-2016学年贵州遵义一中高二下第二次联考理综化学卷(解析版) 题型:选择题
下列物质既能与金属钠反应放出气体,又能与纯碱作用放出气体的是( )
A.CH3CH2OH B.H2O C.C6H12O6 D.CH3COOH
查看答案和解析>>
科目: 来源:2015-2016学年贵州遵义一中高二下第二次联考理综化学卷(解析版) 题型:选择题
煤是工业的粮食,石油是工业的血液。下列关于煤和石油的说法错误的是( )
A.石油裂解主要目的是得到短链的不饱和烃
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤的气化与液化都是化学变化
D.煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com