
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
C(s)+H2O(g) CO(g)+H2(g)在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量 B.将容器的体积缩小一半
C.保持容器压强不变,充入N2 D.保持容器体积不变,充入H2O(g)
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
标准状况下,使NO2和O2按4:1的体积比充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度为( )
A. mol•L-1 B.
mol•L-1 B.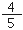 mol•L-1 C.
mol•L-1 C.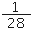 mol•L-1 D.
mol•L-1 D.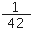 mol•L-1
mol•L-1
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐
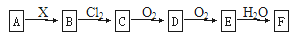
下列说法中不正确的是( )
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.当X是强酸时,C在常温下是气态单质
D.B和Cl2的反应是氧化还原反应
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
向Ba(OH)2溶液中逐滴加入稀硫酸,若缓缓加入稀硫酸直至过量,整个过程中混合溶液中的导电能力(用I表示)可近似地用下图中的曲线表示的是

A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
下列现象中,是因为发生加成反应而产生的现象是
A.乙烯使溴的四氯化碳溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使酸性高锰酸钾溶液褪色
D.甲烷与氯气混合,光照一段时间后黄绿色消失
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是( )

A.N4分子属于一种新型的化合物 B.N4分子中只含有非极性键
C.1molN4分子所含共价键数为4NA D.N4沸点比P4(白磷)高
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
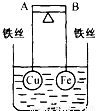
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D.当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
一定温度下,在容积恒定的密闭容器中进行反应A(s)+2B(g) C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
①混合气体的密度不变
②容器内气体的压强不变
③混合气体的总物质的量不变
④B的物质的量浓度不变
⑤v正(C)=v逆(D)
⑥v正(B)=2v逆(C)
A.①④⑤⑥ B.②③⑥ C.②④⑤⑥ D.只有④
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:选择题
A、B两种有机化合物,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧时产生的CO2的量均相等,符合上述条件的是( )
①同分异构体;②同系物;③具有相同的最简式;④含碳的质量分数相同
A.①③④ B.①③ C.①②③④ D.①②④
查看答案和解析>>
科目: 来源:2015-2016学年湖北省枣阳市高一5月月考化学试卷(解析版) 题型:填空题
Ⅰ:下列各项分别与哪个影响化学反应速率因素的关系最为密切?
(1)夏天的食品易变霉,在冬天不易发生该现象 ;
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢 ;
(3)MnO2加入双氧水中放出气泡更快 .
Ⅱ:在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
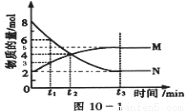
(1)比较t2时刻,正逆反应速率大小V正 V逆.(填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为: .
(3)t3时刻化学反应达到平衡,反应物的转化率为 .
(4)如果升高温度,则V逆 (填增大、减小或不变).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com