
科目: 来源:2016届安徽省高三下学期冲刺模拟理综化学A卷(解析版) 题型:实验题
[化学一选修5:有机化学基础]
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
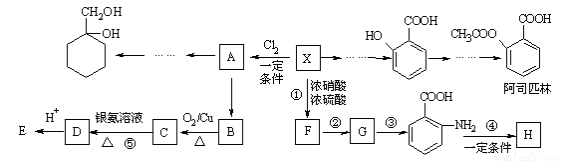
已知:Ⅰ.
Ⅱ.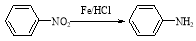 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)X的分子式是 。
(2)H的结构简式是 。
(3)反应②③的类型是 、 。
(4)反应⑤的化学方程式是__________________________________。
(5)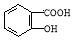 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 种。
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 种。
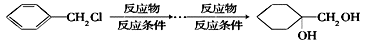
(6)请用合成反应流程图表示出由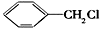 和其他无机物合成
和其他无机物合成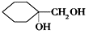 的最合理的方案(不超过4步)。例如:
的最合理的方案(不超过4步)。例如:
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
下列说法错误的是
A.葡萄糖可用于合成葡萄糖酸钙口服液
B.工业制普通玻璃的原料是石英、纯碱、石灰石
C.月饼包装盒中常放入生石灰或硅胶做干燥剂,铁粉或硫酸亚铁做抗氧化剂
D.原子利用率=期望产物的原子总数与生成物原子总数之比
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
2015年诺贝尔生理学或医学奖授予中国药学家屠呦呦以及爱尔兰科学家威廉·坎贝尔和日本科学家大村智,表彰他们在寄生虫疾病治疗研究方面取得的成就。屠呦呦先驱性地发现了青蒿素,开创了疟疾治疗新方法。右图为青蒿素,关于该物质的下列说法正确的是
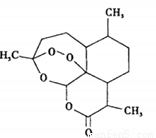
A.青蒿素化学式为C15H20O5
B.在光照条件下可能发生取代反应
C.可以与氢气发生加成反应
D.水浸青蒿对治疗疟疾有良好的疗效
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O
B.浓烧碱溶液中加入铝片:Al + 2OH-=AlO2-+H2↑
C.氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓
D.用惰性电极电解氯化镁溶液:Mg2++2Cl-+2H2O Cl2↑+H2↑+Mg(OH)2↓
Cl2↑+H2↑+Mg(OH)2↓
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值,下列叙述正确的是
A.1mol Na2O2与足量的水反应,转移的电子数为2NA
B.17g羟基中含有的电子数为10NA
C.标准状况下,1mol已烷中共价键数目为19NA
D.1L 0.10mol·L-1的Na2CO3溶液中阴离子数目之和小于0.1NA
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
分子式C4H8O为并能与金属Na反应放出气体的单官能团的有机物(不含立体异构)有
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
下列有关物质结构的说法正确的是
A.电子层数多的原子的半径一定大于电子层数少的原子的半径
B.P4S3分子中各原子的最外层均已达到了8电子稳定结构,则分子中共价键数目为9条
C.H2SO3酸性强于H2CO3,所以非金属性S大于C
D.不同原子形成的共价键一定是极性键
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A.向蛋白质溶液中滴加饱和Na2SO4溶液或浓硝酸均会产生白色沉淀,是因为蛋白质变性
B.提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法
C.某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水,石灰水变浑浊,该钾盐一定是K2CO3
D.进行K与水反应的实验操作:可在培养皿中放些水,然后取绿豆大小的钾,用滤纸吸干表面的煤油,投入培养皿中
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:实验题
某粗铜含铁、金和铅等杂质,通过电解精炼铜后,阳极泥含有Cu、Au(金)和PbSO4等杂质,为充分利用电解后的阳极泥和电解液,设计如下工艺流程:
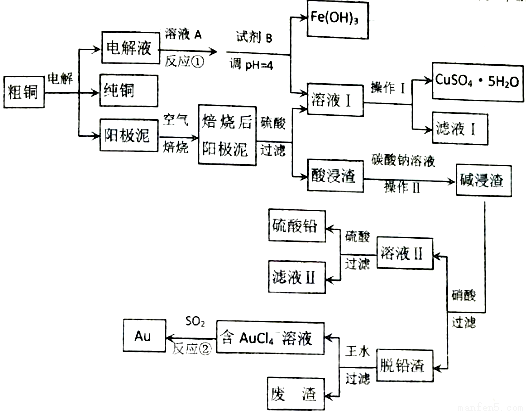
回答下列问题:
(1)溶液A是一种绿色氧化剂,则反应①的离子方程式为
(2)试剂B为
(3)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 (写一点即可)。
(4)操作Ⅰ的主要步骤为 过滤,洗涤,干燥
(5)写出反应②的离子方程式 。
(6)为了减少废液排放、充分利用有用资源,工业上将滤液Ⅰ并入溶液Ⅰ进行循环操作,请指出流程图中另一处类似的做法 。
(7)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)=1.2×10-8,用离子方程式表示加入碳酸钠溶液的作用 。
查看答案和解析>>
科目: 来源:2016届辽宁省高三第七次模拟理综化学试卷(解析版) 题型:实验题
Ⅰ.Fe3+具有氧化性,实验室测定含碘废液中I-的含量的过程如下:量取25.00 mL废液于250 mL锥形瓶中,分别加入5 mL 2 mol·L-1 H2SO4和10 mL 20% Fe2(SO4)3溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入几滴二苯胺磺酸钠(用作指示剂),用0.02500 mol·L-1标准K2Cr2O7溶液进行滴定到终点。重复3次,数据记录如下表:
次数 | 1 | 2 | 3 |
滴定体积/mL | 19.98 | 20.02 | 19.00 |
(1)在盛有废液的锥形瓶中先加入5 mL 2 mol·L-1 H2SO4的目的是
______________________________。(用离子方程式和语言叙述解释)
(2)上述过程中涉及的反应:①2Fe3++2I-===2Fe2++I2 ②______________________________。
(3)根据滴定有关数据,该废液中I-含量是_____g·L-1。
(4)在滴定过程中,下列操作(其他操作正确)会造成测定结果偏低的是___________。
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗衣后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡
Ⅱ.Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点。某学习小组同学设计如下实验:
实验编号 | 实验操作 | 现象 |
1 | 向10mL 3mol/L KNO3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 无白色沉淀生成 |
2 | 向10mL 1mol/L AgNO3溶液中滴加2mL 0.1mol/L FeSO4溶液,振荡,再滴加酸性KMnO4溶液 | 紫红色不褪去 |
3 | 向10mL 1mol/L Fe(NO3)3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 有白色沉淀生成 |
请回答:
(5)设计实验①的目的是______________________________。
(6)实验③可得出结论是______________________________。
(7)写出实验②中反应的离子方程式______________________________。
(8)根据以上实验,Fe3+和Ag+的氧化性相对强弱与离子____________________有关。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com