
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
生产、生活中处处有化学,下列有关说法正确的是
A.工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料
B.某雨水样品放置一段时间后,PH由4.68变为4.00,是因为水中溶解的CO2增多
C.在结冰的路面上撒盐,是利用盐与水发生化学反应放出大量热量,促使冰雪融化
D.人类对于能源的利用大致可以分为三个时代:柴草能源、化石能源、多能源时代,目前,全球已主要处于多能源时代
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是
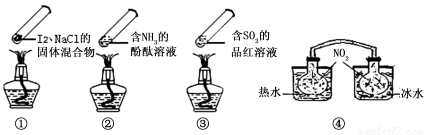
A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差
B.加热时,②、③中的溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅
D.四个“封管实验”中都有可逆反应发生
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
第三周期元素,浓度均为0.01 mol/L的最高价氧化物对应水化物的pH与原子半径的关系如右图所示。则下列说法正确的是

A.气态氢化物的稳定性:N>R
B.Z的最高价氧化物对应的水化物能溶于稀氨水
C.Y和R形成的化合物既含离子键又含共价键
D.X和M两者最高价氧化物对应的水化物恰好完全反应后溶液的pH>7
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
石墨烯可看作将石墨的层状结构一层一层地剥开得到的单层碳原子;石墨炔是平面网状结构的全碳分子,具有优良的化学稳定性和半导体性能,还可用于H2的提纯;将氢气氢化到石墨烯排列的六角晶格中,使每个碳原子都增加一个氢原子可得最薄的绝缘新材料石墨烷。下列有关说法中不正确的是
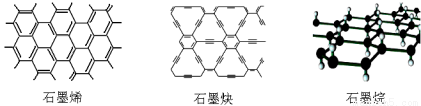
A.石墨烯和石墨炔互为同素异形体
B.石墨炔有望替代二氧化硅用作半导体材料
C.12g石墨烯完全转变为石墨烷需标况下11.2L氢气
D.石墨炔孔径略大于H2分子的直径,因此它是理想的H2提纯薄膜
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
已知: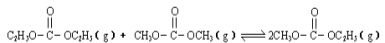 是碳酸甲乙酯的工业生产原理。下图是投料比[
是碳酸甲乙酯的工业生产原理。下图是投料比[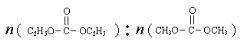 ]分别为3:1和1:1、反应物的总物质的量相同时,
]分别为3:1和1:1、反应物的总物质的量相同时,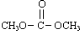 的平衡转化率与温度的关系曲线。下列说法正确的是
的平衡转化率与温度的关系曲线。下列说法正确的是
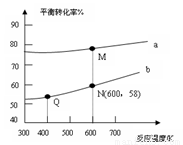
A.曲线b所对应的投料比为3:1
B.M点对应的平衡常数小于Q点
C.N点对应的平衡混合气中碳酸甲乙酯的物质的量分数为0.58
D.M点和Q点对应的平衡混合气体的总物质的量之比为2:1
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
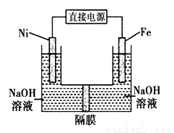
A.镍是阳极,电极反应为4OH--4e一= O2↑+ 2 H2O
B.电解时电流的方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
下列有关电解质溶液的叙述正确的是
A.常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7,则滤液中: c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2c(CO32-)
B.40℃时,在氨水体系中不断通入CO2,随着CO2的通入,不断增大
C.室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入0.05molCaO,所得溶液中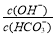 增大
增大
D.为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2 。用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·x H2O的化学方程式为
(2)玻璃棒有多种用途,下列实验操作中玻璃棒的作用完全相同的是 (填字母)
①测定醋酸钠溶液的pH ②加热食盐溶液制备NaCl晶体
③配制0.1mol/L的硫酸溶液 ④用淀粉—KI试纸检验溶液中氧化性离子
⑤配制10%的硫酸钠溶液
A.①⑤ B.②⑤ C.①④ D.③④
(3)水洗时检验TiO2·x H2O已洗净的方法是
(4)下列可用于测定TiO2粒子大小的方法是 (填字母代号)
a.核磁共振氢谱 b.红外光谱法 c.质谱法 d.透射电子显微镜法
(5)滴定终点的现象是
(6)滴定分析时,称取TiO2(摩尔质量为Mg·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为 %
(7)下列操作会导致TiO2质量分数测定结果偏高的是
A. 滴定终点读取滴定管刻度时,俯视标准液液面
B. 配制标准溶液时,烧杯中的NH4Fe(SO4)2溶液有少量溅出
C. 容量瓶清洗之后,未干燥
D.配制标准溶液定容时,俯视刻度线
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
Ⅰ.改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气。
(1)已知:H2(g)+1/2O2(g)═H2O(g) △H1= —241.8 kJ•mol-1
2C(s)+O2(g)═2CO(g) △H2= —221 kJ•mol-1
由此可知焦炭与水蒸气反应的热化学方程式为
(2)煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为
(已知:H2S:Ka1=1.3×10-7,Ka2=7.1×10-15;H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11)
(3)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH,得到两组数据
CO2(g)+H2(g) ΔH,得到两组数据
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡 所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
该反应的 H 0(填“<”或“>”);若在9000C时,另做一组实验,在2L的恒容密闭容器中加入l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2,则此时?正 ?逆(填“<”,“>”,“=”)。
H 0(填“<”或“>”);若在9000C时,另做一组实验,在2L的恒容密闭容器中加入l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2,则此时?正 ?逆(填“<”,“>”,“=”)。
(4)一定条件下,某密闭容器中已建立A(g)+B(g)
C(g)+D(g) △H>0的化学平衡,其时间速率图像如右图,下列选项中对于t1时刻采取的可能操作及其平衡移动情况判断正确的是
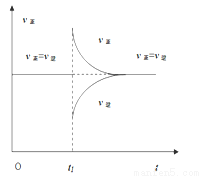
A.减小压强,同时升高温度,平衡正向移动
B.增加B(g)浓度,同时降低C(g)浓度,平衡不移动
C.增加A(g)浓度,同时降低温度,平衡不移动
D.保持容器温度压强不变通入稀有气体,平衡不移动
Ⅱ.压缩天然气(CNG)汽车的优点之一是利用催化技术将NOx转变成无毒的CO2和N2。
①CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) △H1<0
2N2(g)+CO2(g)+2H2O(g) △H1<0
②CH4(g) +2NO2(g) N2(g) +CO2(g) +2H2O(g) △H2<0
N2(g) +CO2(g) +2H2O(g) △H2<0
(5)收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V (NO)︰V (NO2)= 。
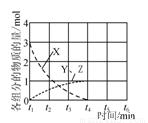
(6)在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示。写出Y和Z的化学式:
查看答案和解析>>
科目: 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:实验题
为减少铬渣的危害并从中提取硫酸钠,设计工艺如下:
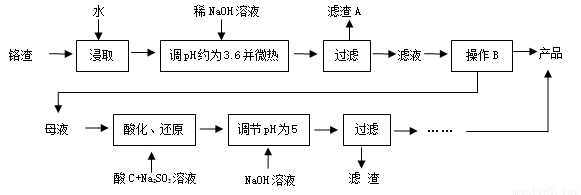
已知:①铬渣含有Na2SO4及少量Cr2O72-、Fe3+
②Fe3+、Cr3+完全沉淀(c≤1.0×10-5mol·L-1)时pH分别为3.6和5。
(1)“微热”的作用:① ;② 。
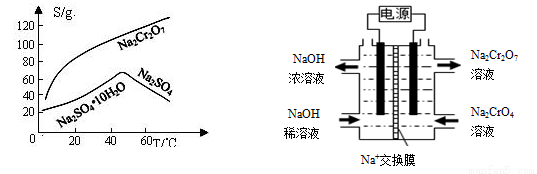
(2)根据溶解度(S)~温度(T)曲线,操作B的最佳方法为 (填字母)
a. 蒸发浓缩,趁热过滤 b. 蒸发浓缩,降温结晶,过滤
(3)酸化后Cr2O72-可被SO32-还原成Cr3+,离子方程式为 ;酸C为 ,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]= 。
(4)已知Cr(OH)3在溶液中存在平衡H++CrO2-(亮绿色)+H2O?Cr(OH)3(s)?Cr3+(紫色)+3OH-,加入NaOH溶液时要控制pH为5,pH不能过高的理由是 。
(5)根据2CrO42-+2H+ Cr2O72-+H2O设计上图装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中左侧电极连接电源的 极,电解制备过程的总反应方程式为 。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为d,则此时Na2CrO4的转化率为 。若选择用熔融K2CO3作介质的甲醇(CH3OH)燃料电池充当电源,则负极反应式为 。
Cr2O72-+H2O设计上图装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中左侧电极连接电源的 极,电解制备过程的总反应方程式为 。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为d,则此时Na2CrO4的转化率为 。若选择用熔融K2CO3作介质的甲醇(CH3OH)燃料电池充当电源,则负极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com