
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
对可逆反应2A(s)+3B(g) C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③缩小反应容器容积压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
下列变化不能用勒夏特列原理解释的是( )
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.工业合成氨的反应,往往需要使用催化剂
C.Fe(SCN)3溶液中加入少量固体KSCN后颜色变深
D.实验室用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
已知碳、一氧化碳、晶体硅的燃烧热分别是△H =-393.5kJ/mol、△H =-283 kJ/mol和△H =-989 kJ/mol,则工业冶炼晶体硅反应2C(s)+SiO2(s)= Si (s)+2 CO(g) 的反应热为( )
A.+768 kJ/mol B.-768 kJ/mol C.+2342 kJ/mol D.-2342 kJ/mol
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
已知:2H2(g)+O2(g)=2H2O(g) △H1
3H2(g)+Fe2O3(s)=2Fe(s)+3H2O(g) △H2
2 Fe(s)+3/2O2(g)=Fe2O3(s) △H3
2Al(s)+3/2O2(g)=Al2O3(s) △H4
2Al(s)+Fe2O3(s)=A12O3(s)+2Fe(s) △H5
下列关于上述反应焓变的判断正确的是( )
A.△H1<0,△H3>0 B.△H5<0,△H4 <△H3
C.△H1=△H2+△H3 D.△H3=△H4+△H5
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
将4 mol A气体和2 mol B气体在2 L的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g) ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
2C(g) ΔH<0,4 s后反应达到平衡状态,此时测得C的浓度为0.6mol/L,下列说法中正确的是( )
A.反应过程中,当A、B、C的物质的量浓度之比为2∶1∶2时,反应即达到平衡状态
B.4 s内用物质B表示的反应速率为0.075 mol/(L·s)
C.达平衡后若增大压强,A的转化率降低
D.达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
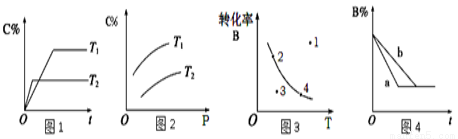
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n﹤p
C.图3中,表示反应速率v正>v逆的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
已知反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是 ( )
2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是 ( )
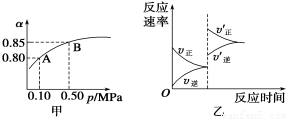
A.由图甲知,A点SO2的平衡浓度为0.4 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
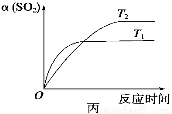
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:选择题
一定温度下,C和H2O(g)在密闭容器中发生下列反应:①C(s)+H2O(g)  CO(g)+H2(g) ②CO(g)+H2O(g)
CO(g)+H2(g) ②CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,测得c(H2)=1.9mol/L,c(CO)=0.1 mol/L,则CO2的浓度为( )
A.0.1 mol/L B.0.9 mol/L C.1.8 mol/L D.1.9mol/L
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:填空题
现有反应mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率减小;当减小压强时,混合体系中A的质量分数增大,则
pC(g),达到平衡后,当升高温度时,B的转化率减小;当减小压强时,混合体系中A的质量分数增大,则
(1)该反应的正反应是__________热反应,且m+n__________p (填“>”、“<”或“=”)。
(2)增大压强时,B的转化率__________(填“增大”、“减小”或“不变”,下同),逆反应速率__________。
(3)若加入C(体积不变),则A的体积分数__________。
(4)若降低温度,则平衡时B、C的浓度之比c(C)/c(B)比值将________。
(5)若加入催化剂,该反应的反应热________。
(6)若B是有色物质,A、C均为无色物质,维持容器体积不变,充入氖气时,混合气体的颜色__________(填“变浅”、“变深”或“不变”)。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江大庆市高一下期中化学试卷(解析版) 题型:填空题
已知:2NO2(g) N2O4(g) △H<0。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
N2O4(g) △H<0。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
(1)a、b、c、d四个点中,化学反应处于平衡状态的是 点。
(2)25 min时,增加了 (填物质的化学式) mol。
(3)a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是 (填字母)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com