
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:选择题
反应A(g)+3B(g)===2C(g)+D(g),在四种不同的情况下,反应速率分别如下,其中该反应进行最快的是
A.v(A)=0.15 mol·(L·s)-1 B.v(B)=0.6 mol·(L·s)-1
C.v(C)=0.6 mol·(L·s)-1 D.v(D)=0.2 mol·(L·s)-1
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.钢铁发生电化学腐蚀时,负极反应都是Fe-3e-= Fe3+
B.镀锡的铁制品,若发生镀层破损,铁制品比受损前更容易锈蚀
C.铜的金属活动性比铁弱,可在海轮外壳上装上铜块以减缓船体腐蚀
D.钢铁发生吸氧腐蚀时,正极反应是:2H2O+O2+4e-= 4OH-
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:选择题
对于合成氨反应N2(g)+3H2(g) 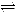 2NH3(g) ?H<0;,下列反应速率关系中,正确的是
2NH3(g) ?H<0;,下列反应速率关系中,正确的是
A.3 v (N2)=v(H2) B.v (N2)=3v(H2)
C.1.5v (H2)=v(NH3) D.v (N2)=2v(NH3)
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列(平衡移动)原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
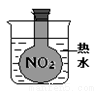
B.将收集NO2气体的烧瓶密闭后,放在装有热水的烧杯中,发生颜色变化
C.合成氨时采用铁触媒作反应催化剂
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:选择题
一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(g) +2B(g)?C(g)+ D(g),观察下列物理量,能表明该反应已达到平衡状态的是
A.C物质的物质的量浓度不变
B.物质C和物质D的物质的量浓度相等
C.B物质的转化率不发生变化
D.反应速率v (A)= v (D)
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:选择题
在恒容的密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是

A.图Ⅰ研究的是t1时刻,升高了反应的温度
B.图Ⅱ研究的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ若是研究不同压强对平衡的影响,且乙反应的压强较高
D.图Ⅲ若是研究不同温度对平衡的影响,且乙的反应温度较高
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:填空题
右图是钢铁在潮湿空气里发生电化学腐蚀的示意图,发生的反应为:
2Fe+2H2O+O2=2Fe(OH)2。Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈。请根据图示,回答下列问题:
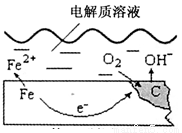
(1)在上述电化学腐蚀中,碳(C)作 极。
(2)写出负极的电极反应式 。
(3)工业上,常在钢铁设备的表面涂一层油,其作用是 。
A.减少钢铁与空气和水的接触,防止在钢铁表面形成微小原电池
B.隔绝钢铁与空气和水的接触,阻止在钢铁表面形成微小电解池
C.润滑设备,防止灰尘污染
D.防止人为接触设备,避免设备腐蚀
(4)如果将长期浸泡在河水中的钢铁闸门与外电源连接防腐,应将闸门连接外部直流电源的 极。
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:填空题
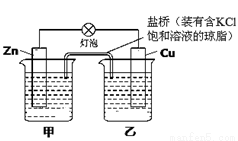
(1)已知Zn+CuSO4=Cu+ZnSO4,设计原电池:构造如下图所示,试问ZnSO4溶液放在 (填“甲”或“乙”)烧杯,盐桥中的离子向两端烧杯移动,构成闭合回路,K+移向 (填“甲”或“乙”)烧杯;
(2)电解饱和食盐水是重要的化工产业,它被称为 “氯碱工业”。在教材《化学1》、《化学2》、《化学反应原理》中均有提及,请写出电解饱和食盐水的化学反应方程式
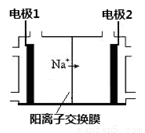
其中右图是《化学反应原理》中电解饱和食盐水工业中所采用的离子交换膜电解槽示意图,部分图标文字已被除去,请根据图中残留的信息,通电以后,Na+向右侧移动,可判断出电极2是 极,在该电极周围的溶液中,NaOH浓度将会 (填“变大”或“减小”或“不变”);电极1上的电极反应式为 。
查看答案和解析>>
科目: 来源:2015-2016学年江苏省宿迁市沭阳县高二下学期期中考试化学试卷(解析版) 题型:填空题
(1)已知热化学方程式:Zn(s)+1/2O2(g) =ZnO(s) △H1;Hg(l)+1/2O2(g) =HgO(s) △H2;
则Zn(s)+HgO(s)=Hg(l)+ZnO(s) △H值为 。(用△H1和△H2的代数式表示)
(2)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl(g)+O2(g)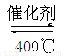 2Cl2(g)+2H2O(g)。若反应中4mol HCl被氧化,放出115.6kJ的热量,且部分化学键断裂示意图如下:
2Cl2(g)+2H2O(g)。若反应中4mol HCl被氧化,放出115.6kJ的热量,且部分化学键断裂示意图如下:
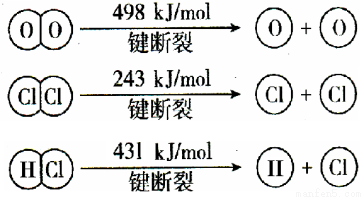
①反应A的热化学方程式是 。
②断开1 mol H—O键,需要吸收的能量为 kJ,H2O中H—O 键与HCl中H—Cl键相比, 的键能较大。(填“H—O”或“H—Cl”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com