
科目: 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:计算题
把3molA和2.5molB混合与2L密闭容器中,发生反应:3A(g)+B(g) xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
(1)x= 。
(2)平衡时C的浓度为多少?(要求写出计算过程)
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷定,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭)。下列说法不正确的是
A.倭铅是指金属锌和铅的混合物 B.煤炭中起作用的主要成分是C
C.冶炼Zn的过程中有氧化还原反应发生 D.该冶炼锌的方法属于热还原法
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.等物质的量的O2和CO2所含氧原子数均为2NA
B.标准状况下,2.24 L一氯甲烷中含有氢原子数目为0.3NA
C.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA
D.6.8 g熔融的KHSO4中含有0.1 NA个阳离子
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。”下列关于青蒿素和双氢青蒿素(结构如图),下列说法错误的是
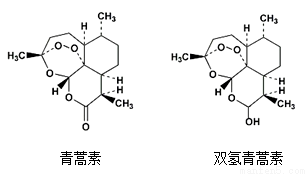
A.青蒿素和双氢青蒿素互为同分异构体
B.由青蒿素制备双氢青蒿素的反应属还原反应
C.青蒿素的分子式为C15H22O5
D.青蒿素分子中含有过氧键和酯基、醚键
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
下列实验中,对应的现象及结论都正确且存在因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 用酒精灯加热摩尔盐(NH4)2Fe(SO4)2•6H2O,产生的气体通过装有无水硫酸铜的干燥管 | 干燥管中的白色粉末先变成天蓝色,后又变成深蓝色 | 加热温度较低时摩尔盐分解产生水蒸气,温度稍高时分解产物中有氨气 |
B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
C | 向CuSO4溶液中通入H2S气体 | 溶液的蓝色褪去,生成黑色沉淀 | 氢硫酸的酸性比硫酸强 |
D | 向2ml0.1mol/LAgNO3溶液中先滴几滴0.1mol/L的NaCl溶液,再滴入几滴0.1mol/L的NaI溶液 | 先生成白色沉淀,后生成黄色沉淀 | 溶度积KSp(AgCl) >KSp(AgI) |
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
瑞典ASES公司设计的曾用于驱动潜艇的液氨—液氧燃料电池示意图如图所示,下列有关说法正确的是
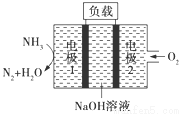
A.电池工作时,Na+向电极1移动
B.电池工作一段时间后停止,溶液pH值不变
C.电极1发生的电极反应为2NH3+6OH--6e-===N2↑+6H2O
D.用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3 的同时阳极会得到19.2g纯铜
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
W、X、Y、Z均为短周期主族元素,Y的原子序数是W和Z的原子序数之和的一半,Y原子的最外层电子数与核外电子总数之比为2︰7;W和Z形成的可溶性化合物WZ溶于水不能促进水的电离;W、X、Z三种元素形成的某种化合物能消毒杀菌,下列说法正确的是
A.四种元素的原子中,原子半径最大的是Z
B.X、Y形成的化合物能溶于盐酸
C.1 mol W单质与足量X单质反应,转移的电子数为2NA
D.Z 的最高价氧化物对应水化物的酸性强于Y的最高价氧化物对应水化物的酸性
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:选择题
常温下,浓度均为0.10 mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是

A.该温度下HB的电离平衡常数a < b
B.溶液中水的电离程度:a=c>b
C.相同条件下NaA溶液的pH小于NaB溶液的pH
D.当 时,若同时微热两种溶液(不考虑HA、HB和H2O的挥发),则
时,若同时微热两种溶液(不考虑HA、HB和H2O的挥发),则 减小
减小
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:实验题
氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸能够引起燃烧。某活动小组准备使用下列装置制备LiH固体。
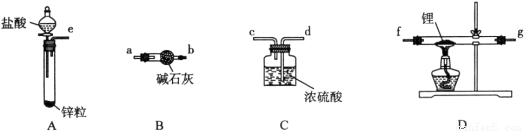
甲同学的实验方案如下:
(1)仪器的组装连接:上述仪器装置接口的连接顺序为____________________,加入药品前首先要进行的实验操作是____________________(不必写出具体的操作方法);其中装置B的作用是________________。
(2)添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯中浸洗数次,该操作的目的是________________________________________,然后快速把锂放入到石英管中。
(3)通入一段时间氢气后加热石英管,在加热D处的石英管之前,必须进行的实验操作是______________________________________________________________________。
(4)加热一段时间后停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险。(反应方程式:
LiH + H2O = LiOH + H2↑),分析该反应原理,完成LiH与无水乙醇反应的化学方程式_________________ ___________________。
(5)准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体0.021mol,则产品中LiH与Li的物质的量之比为____________________。
(6)乙同学对甲的实验方案提出质疑,他认为未反应的H2不能直接排放,所以在最后连接了装置E用来收集H2,请将E装置补充完整。
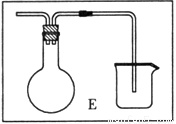
查看答案和解析>>
科目: 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:简答题
综合利用CO2、CO对构建低碳社会有重要意义。
(1) Li4SiO4可用于富集得到高浓度CO2。原理是:在500℃,低浓度CO2与Li4SiO4接触后生成两种锂盐;平衡后加热至700℃,反应逆向进行,放出高浓度CO2,Li4SiO4再生。700℃时反应的化学方程式为_________________________________。
(2) 固体氧化物电解池(SOEC)用于高温电解CO2和H2O,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如右图。

① b为电源的________(填“正极”或“负极”)。
② 写出电极c发生的电极反应式: __________ ______、 __________________ ______。
(3)电解生成的合成气在催化剂作用下发生如下反应:CO(g)+2H2(g)  CH3OH(g)。对此反应进行如下研究:
CH3OH(g)。对此反应进行如下研究:
某温度下在一恒压容器中分别充入1.2 mol CO和1 mol H2,达到平衡时容器体积为2 L,且含有0.4 mol CH3OH(g),则该反应平衡常数值为________,此时向容器中再通入0.35 mol CO气体,则此平衡将________(填“向正反应方向”“不”或“向逆反应方向”)移动。
(4) 已知:

若甲醇的燃烧热为ΔH3,试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)  CH3OH(l)的ΔH,
CH3OH(l)的ΔH,
则ΔH=______ ____。
(5)利用太阳能和缺铁氧化物[如Fe0.9O]可将廉价CO2热解为碳和氧气,实现CO2再资源化,转化 过程如下图所示,若用1 mol缺铁氧化物[Fe0.9O]与足量CO2完全反应可生成________mol C(碳)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com