
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:选择题
依据下列实验现象,得出的结论正确的是 ( )
选项 | 操作 | 实验现象 | 结论 |
A | 向NaBr溶液中加入氯水,再加入淀粉?KI溶液 | 溶液变蓝 | 氧化性:Cl2>Br2>I2 |
B | 将铝片放入盐酸中 | 产生气泡的速率开始较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜悬浊液,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性或蔗糖未水解 |
D | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值,下列叙述正确的是( )
A.1molFeI2与足量的氯气反应转移电子数为2NA
B.标准状况下22.4L一氯甲烷和二氯甲烷的混合物中所含氯原子数介于NA至2NA之间
C.0.1molCu与足量热的浓硫酸反应生成的SO2体积标准状况下约为2.24L
D.0.2mol/L的Na2S溶液中,所含S2-数目小于0.2NA
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:选择题
下列实验所对应的离子方程式正确的是( )
A.向漂白粉溶液中通入SO2:Ca2++ClO-+SO2+H2O=CaSO3↓+ 2HClO
B.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.在碳酸氢钡溶液中加入过量的氢氧化钠溶液:Ba2++2HCO+2OH-=BaCO3↓+CO+2H2O
D.向Na2S2O3溶液中加入稀硫酸:S2O32-+4H+=SO42-+3S↓+2H2O
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:选择题
甲苯苯环上的一个H原子被-C3H6Cl取代,形成的同分异构体有(不考虑立体异构) ( )
A.9种 B.12种 C.15种 D.18种
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:选择题
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀。如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2(OH)3Cl 。
下列说法不正确的是( )
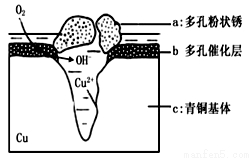
A. 腐蚀过程中,负极 a被氧化
B. 环境中的Cl-扩散到孔口,并与正极反应产物和负极
反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
C. 若生成 2.145gCu2(OH)3Cl,则理论上消耗标准状况氧气体积为 0.448L
D. 正极的电极反应式为: 正极反应是 O2+ 4e-+2H2O=4OH-
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:选择题
已知25 ℃时,几种弱酸的电离常数如下:
弱酸的化学式 | CH3COOH | HCN | H2S |
电离常数 | 1.8×10-5 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
25 ℃时,下列说法正确的是( )
A.等物质的量浓度的各溶液pH关系为:pH(Na2S)>pH(NaCN) >pH(NaHS)>pH(CH3COONa)
B.用0.1mol/L的NaOH溶液滴定pH值相等的CH3COOH和HCN溶液,CH3COOH消耗的NaOH溶液体积更大
C.NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)+c(H2S)
D.某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-d mol/L
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:简答题
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)在固定体积的密闭容器中,进行如下化学反应: N2(g)+3H2(g)  2NH3(g)
2NH3(g)  H=-92.4 kJ/mol,其平衡常数K与温度T的关系如下表:
H=-92.4 kJ/mol,其平衡常数K与温度T的关系如下表:
T/K | 298 | 398 | 498 |
平衡常数K | 4.1×106 | K1 | K2 |
①试判断K1 K2(填写“>”“=”或“<”)。
②如果合成氨反应的方程式写为 N2(g)+
N2(g)+  H2(g)
H2(g) NH3(g),其平衡常数为K’,则K’与K的关系为_________(填字母)
NH3(g),其平衡常数为K’,则K’与K的关系为_________(填字母)
A.K’ = K B.K’ = 2K C. K’ =  K D.K’ =
K D.K’ = 
(2)下列各项能说明合成氨反应已达到平衡状态的是 (填字母)(反应是在固定体积的密闭容器中进行的)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.v(N2)(正) = 3v(H2)(逆)
c.容器内压强保持不变 d.混合气体的密度保持不变
e.混合气体的平均摩尔质量不变
(3)将0.3 mol N2和0.5 mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,测得容器内气体压强变为原来的 ,此时H2的转化率为 ;欲提高该容器中H2的转化率,下列措施可行的是 (填选项字母)。
,此时H2的转化率为 ;欲提高该容器中H2的转化率,下列措施可行的是 (填选项字母)。
A.向容器中按原比例再充入原料气 B.向容器中再充入一定量H2
C.改变反应的催化剂 D.液化生成物分离出氨
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式 ;
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
C.2 c(N2H62+)+ c([N2H5·H2O] +)= c(H+)+c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:简答题
氮化硅硬度大、熔点高、不溶于酸(氢氟酸除外),是一种重要的结构陶瓷材料。一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的工艺流程如下:
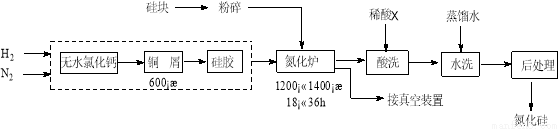
(1)净化N2和H2时,铜屑的作用是: ;硅胶的作用是 。
(2)在氮化炉中3SiO2(s)+2N2(g)=Si3N4(s) △H=-727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度: ;体系中要通入适量的氢气是为了 。
(3)X可能是 (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(4)如何说明氮化硅产品已用水洗干净? 。
(5)用硅粉作硅源、叠氮化钠(NaN3)作氮源,直接燃烧生成氮化硅(发生置换反应),该反应的化学方程式为: 。
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:实验题
中学常采用高锰酸钾加热分解法制取氧气,某兴趣小组经查阅资料获知:制得氧气后固体残余物中的锰酸钾(K2MnO4)具有强氧化性,与还原剂、有机物、易燃物混合可形成爆炸性混合物,如不妥善处置将造成危险。因此该小组对该残余物进行分离提纯,得到锰酸钾晶体,利用回收的锰酸钾与浓盐酸反应制取氯气,并设计实验验证氯气化学性质。

(1)打开分液漏斗活塞及弹簧夹2,观察到烧瓶壁有紫红色物质生成并逐渐消失,黄绿色气体充满烧瓶。反应结束后,烧瓶内有黑色固体残余,写出过程中发生的化学反应方程式: 。
(2)该小组利用装置C吸收氯气制备漂白粉。
①C中盛装的试剂为 。
②陶瓷多孔球泡的作用是 。
(3)测定漂白粉有效成分的质量分数:称取1.5g所制漂白粉配成溶液,调节pH值并加入指示剂,用0.1000mol/L KI溶液进行滴定,三次平行实验平均每次消耗20.00ml标准液时达到滴定终点,反应原理涉及到的方程式为:
3ClO-+I-=3Cl-+ IO3- IO3-+5I-+3H2O=6OH-+3I2
①所选的指示剂为 ,达到滴定终点的标志是 。
②该漂白粉中有效成分的质量分数为 。
(4)打开分液漏斗活塞及弹簧夹1,可观察到D中的现象为 ,该现象能够证明氯气有氧化性。甲同学认为取D中反应后溶液,滴加硝酸酸化的硝酸银,若有白色沉淀产生,也能证明氯气氧化了亚硫酸氢钡,你认为是否正确并说明理由 。
查看答案和解析>>
科目: 来源:2016届辽宁省高三下第四次模拟理综化学试卷(解析版) 题型:简答题
【化学---选修2:化学与技术】水是生命之源,水的品质对于健康有着十分重要的意义。化学兴趣小组对某山泉水进行分析化验,结果显示水的硬度为28°(属于硬水),主要含钙离子、镁离子、氯离子和硫酸根离子。请思考下列问题:
(1)该泉水属于 硬水(填写“暂时”或“永久”)。
(2)若要除去Ca2+、Mg2+可以往水中加入石灰和纯碱,试剂添加时先加 后加 ,原因是 。
(3)目前常用阳离子交换树脂如NaR、HR来进行水的软化,若使用HR作为阳离子交换树脂则水中的Ca2+、Mg2+与交换树脂的 起离子交换作用。若使用NaR作为阳离子交换树脂失效后可放入5%-8% 溶液中再生。
(4)海水淡化是获得淡水的重要来源。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、S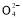 等离子,电极为惰性电极。请分析下列问题:
等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指 (填A或B)。
②写出通电后阳极区的电极反应式 。阴极区的现象是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com