
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列各溶液中,微粒的物质的量浓度关系表述正确的是
A.0.1 mol·L-1 Na2CO3溶液中:c(Na+)=c(HCO3—)+c(H2CO3)+2c(CO32—)
B.pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等
C.将0.2 mol·L-1 NaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中
c(Na+)+c(H+)=c(A-)+c(Cl-)
D.常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7
查看答案和解析>>
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:简答题
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式 。
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。
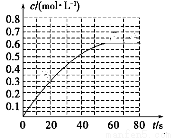
①298K时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 。
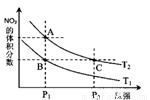
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol 、n(N2O4)=1.2mol,
则此时V(正) V(逆)(填“>”、“<”或“=”)。
 (3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
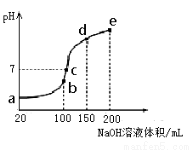
①水的电离程度最大的是 ;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数
K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是
。
查看答案和解析>>
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:实验题
硫化锌 (ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
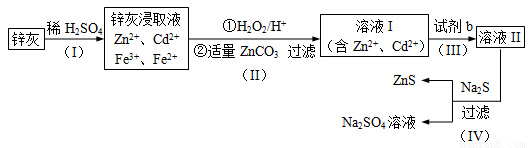
(1)为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 (写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为________;
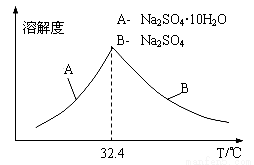
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是 。
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
查看答案和解析>>
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:实验题
制备溴苯的实验装置如下图,将液溴从恒压滴液漏斗慢慢滴入盛有苯和铁粉的烧瓶A。反应结束后,对A中的液体进行后续处理即可获得溴苯。

(1)写出A中制备溴苯的化学反应方程式 。
(2)B中盛放的CCl4的作用是 。
(3)冷凝管的作用是 ,冷凝管中的水应从 口进入(填“a”或“b”)。
(4)向C中加入硝酸银溶液可证明苯和液溴发生的是取代反应而不是加成反应,反应现象是 ,也可使用 试纸更简便地证明上述结论。
(5)得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗,正确的操作顺序是 (填字母标号)。
a.①②③④② b.②④②③① c.④②③①② d.②④①②③
查看答案和解析>>
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:简答题
【化学—选修2 化学与技术】
Ⅰ.下列有关叙述正确的是( )
A.碱性锌锰电池中,MnO2是催化剂
B.银锌纽扣电池工作时,Ag2O被还原为Ag
C.放电时,铅酸蓄电池中硫酸浓度不断增大
D.电镀时,待镀的金属制品表面发生还原反应
Ⅱ.锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌,某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:
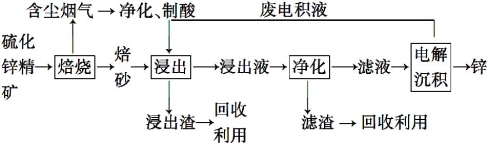
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 。
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的 操作。
(3)浸出液“净化”过程中加入的主要物质为 ,其作用是 。
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气是 。
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生主要反应的离子方程式为 。
(6)我国古代曾采用“火法”工艺冶炼锌,明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,……,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”该炼锌工艺过程主要反应的化学方程式为 。(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
查看答案和解析>>
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:填空题
【化学—选修3 物质结构与性质】
周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子。工业上通过分离液态空气获得X单质。Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和。Z基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)Z2+基态核外电子排布式为________________。
(2)YX4-的空间构型是_______;与YX4-互为等电子体的一种分子为_______(填化学式);HYX4酸性比HYX2强,其原因是____________________。
(3)结构简式为RX(W2H3)2的化合物中R原子的杂化轨道类型为_______;1molRX(W2H3)2分子中含有σ键数目为_______________。
(4)往Z的硫酸盐溶液中通入过量的WH3,可生成[Z(WH3)4]SO4,下列说法正确的是_______。
A.[Z(WH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(WH3)4]2+中Z2+给出孤对电子,WH3提供空轨道
C.[Z(WH3)4]SO4组成元素中第一电离能最大的是氧元素
(5)某Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子)。

①该晶体的化学式为 。
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于 (填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg.cm-3,阿伏加德罗常数为NA,则该晶体中Z原子和Y原子之间的最短距离为 pm(只写计算式)。
查看答案和解析>>
科目: 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:推断题
【化学—选修5有机化学基础】
高分子材料PET聚酯树脂和PMMA的合成路线如下:
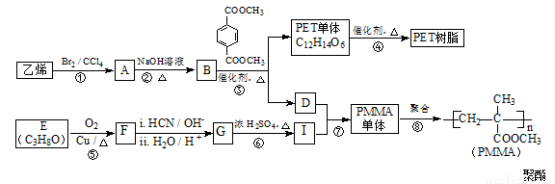
已知:
Ⅰ. RCOOR’+ R”18OH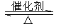 RCO18OR”+R’OH(R、R’、R”代表烃基)
RCO18OR”+R’OH(R、R’、R”代表烃基)

 Ⅱ.
Ⅱ. 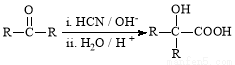 (R、R’代表烃基)
(R、R’代表烃基)
(1)①的反应类型是________。
(2)②的化学方程式为________。
(3)PMMA单体的官能团名称是________、________。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为________。
(5)G的结构简式为________。
(6)下列说法正确的是________(填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d. 1 mol 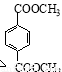 与足量NaOH溶液反应时,最多消耗4 mol NaOH[
与足量NaOH溶液反应时,最多消耗4 mol NaOH[
(7)写出由PET单体制备PET聚酯并生成B的化学方程式________。
查看答案和解析>>
科目: 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关。下列说法正确的是
A.用钢瓶储存液氯或浓硫酸
B.对石油进行分馏可以得到许多苯的同系物
C.汽车尾气中氮氧化物的产生主要是由于汽油中含有氮元素而产生的
D.在某爆炸事故救援现场,消防员发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭
查看答案和解析>>
科目: 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列说法正确的是
A.0.1mol 离子含有的电子、中子数均为1.0NA
离子含有的电子、中子数均为1.0NA
B.标准状况下,4.48L己烷含有的分子数为0.2NA
C.总质量为5.6g的CaO和CaC2混合物中,所含离子总数小于0.2NA
D.常温常压下,0.1molNH3与0.1molHCl充分反应后所得产物含0.1NA个分子
查看答案和解析>>
科目: 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:选择题
A的分子式为C4H10O3,1molA与足量的Na反应会生成1.5molH2,则符合条件的A的结构有(一个C上连多个—OH不稳定,不考虑立体异构)
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com