
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:选择题
原子结构决定元素的性质,下列说法中正确的是
A.Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小,
B.在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的其沸点也一定最高
C.第二周期元素的最高正化合价都等于其原子的最外层电子数
D.非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强
查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:选择题
有机物Q的分子式为C5H10O3,一定条件下Q遇NaHCO3、Na均能产生气体,且生成气体体积比(同温同压)为1:1,则Q的结构最多有( )
A.12种 B.10种 C.8种 D.7种
查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:选择题
利用下列实验装置能完成相应实验的是
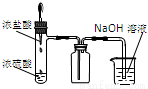
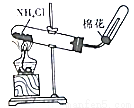
A.制取并收集HCl B.实验室制氨气
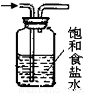
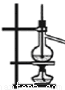
C.除去氯气中的氯化氢 D.分离液体混合物
查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:选择题
室温下进行相关实验。下列结论正确的是
A.向NaHCO3溶液中通CO2至pH=7:c(Na+)=c(HCO3-)+c(CO32-)
B.向CH3COONa溶液中加入等浓度等体积的盐酸:c(Na+)>c(Cl-)
C.向浓度为0.1mol/LNaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH<13
D.将0.1molAgCl投入到100mL0.1mol/LNaCl溶液中:c(Ag+)=c(Cl-)
查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:填空题
二十一世纪钛将成为铁、铝之后的第三大金属,工业上以钛铁矿为原料制备二氧化钛及钛的工艺流程如下图所示,钛铁矿的主要成分为钛酸亚铁(FeTiO3),其中一部分铁元素在风化过程中会转化为+3价,FeTiO3溶于酸后Ti元素以TiO2+存在,TiOSO4遇水可水解。

请根据以上信息回答下列问题:
(1)②中加入铁粉的目的是__________;
(2)③中混合物分离的依据是________(填字母序号)。
a.熔、沸点差异 b.溶解性差异 c.氧化性、还原性差异
(3)②、③、④中均需要进行的操作是________(填操作名称)。
(4)写出④的离子方程式:_______________;该过程在热水中操作的目的是_________
(5)利用生产过程中的废液与软锰矿(主要成分为MnO2)反应可生产硫酸锰(MnSO4,易溶于水),该反应的离子方程式为_______________。
(6)科学家从电解冶炼铝的工艺得到启发.找出了冶炼钛的新工艺。
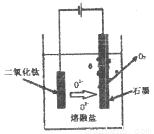
①直接电解固体TiO2法生产钛,原理如图所示,则阴极获得钛的电极反应为_____________。
②电解一段时间后,需要更换石墨电极,原因是_____________。
查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:填空题
氢气是清洁的能源,也是重要的化工原料,根据以下两种制氢方法。完成下列问题:
(1)方法一:H2S热分解法,反应式为:2H2S(g)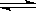 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H
在恒容密闭容器中,测定H2S分解的转化率(H2S的起始浓度均为cmol/L),测定结果见右图,图中曲线a表示H2S的平衡转化率与温度关系,曲线表示不同温度下反应经过相同时间未达到化学平衡时H2S的转化率。
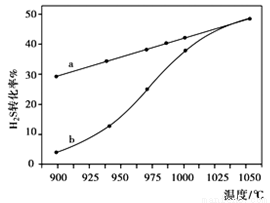
①△H______0,(“>”、“<”或“=”),
②若985℃时,反应经tmin达到平衡,此时H2S的转化率为40%,则tmin内反应速率v(H2)=______(用含c、t的代数式表示)。
③请说明随温度的升高,曲线b向曲线a接近的原因:______。
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.相关主要反应如下:
I:C(s)+H2O(g)═CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g) △H=-43kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(s) △H=-178.3kJ/mol
①计算反应C(s)+2H2O(g)+CaO(s)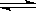 CaCO3(s)+2H2(g)的△H=______;
CaCO3(s)+2H2(g)的△H=______;
若K1、K2、K3分别为反应I、Ⅱ、Ⅲ的平衡常数,该平衡常数K=_____________(用K1、K2、K3表示)。
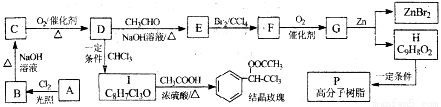
②对于可逆反应C(s)+2H2O(g)+CaO(s)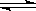 CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是______。(填字母编号)
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是______。(填字母编号)
A.降低体系的温度
B.压缩容器的体积
C.适当增加水蒸气的通入量
D.增加CaO的量
③下图为反应I在一定温度下,平衡时各气体体积百分含量随压强变化的关系图。若反应达某一平衡状态时,测得c(H2O)=2c(H2)=2c(CO)=2mol/L,试根据H2O的体积百分含量变化曲线,补充完整CO的变化曲线示意图。

查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:实验题
四氯化锡(SnCl4)是合成有机锡化合物的原料,其熔点为-33℃,沸点为114℃,在潮湿的空气中强烈水解产生有刺激性的白色烟雾,产物之一为SnO2.实验室制备四氯化锡的操作是:将金属锡熔融,然后泼入冷水,制成锡花,将干燥的锡花加入反应器中;再向反应器中缓慢地通入干燥的氯气。
Ⅰ.图1示实验室制备干燥氯气的实验装置(夹持装置己略)
(1)该装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO)2]和浓盐酸,A中发生反应的化学方程式为_____________。
(2)装置B中的饱和食盐水能够除去Cl2中的HCl,此外还有_____________作用。
(3)试剂X可能为_____________(填写字母).
A.无水氯化钙 B.浓硫酸 C.碱石灰 D.五氧化二磷
(4)四氯化锡在潮湿空气中水解的化学方程式_____________。
(5)用锡花代替锡粒的目的是_____________。
II.图2是蒸馏SnCl4的装置
(6)该装置尚有两处不当之处,它们分别是_____________、_____________。
(7)实验用的锡花中含有金属铜。甲同学设计下列实验测定锡花的纯度。
第一步:称取7.500g锡花溶于足量稀硫酸中,充分反应后过滤;
第二步:向滤液中加入过量Fe2(SO4)3,将生成的Sn2+氧化成Sn4+;
第三步:用1.000mol/LK2Cr2O7溶液滴定生成的Fe2+,发生反应的方程式为(未配平):
Fe2++Cr2O72-+H+→Cr3++Fe3++H2O
若达到滴定终点时共消耗20.00mlK2Cr2O7溶液,试计算锡花中锡的百分含量_____________(结果保留三位有效数字)。
查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:填空题
Q、R、T、W、X、Y、Z为原子序数依次增大的前四周期元素,其中R、T、W是同周期相邻元素,Q、R最外层电子排布可表示为asa,bsbbpa(a≠b):X的基态原子中占据哑铃形原子软道的电子数为10,Y与X为同周期主族元素,基态Z原子核外电子填充在7个能级中,且价层电子有3对成对电子。
(1)四种分子①RY3②TQ4③WQ3④Q2X键角由大到小排列的顺序是_____________(填序号).
(2)微粒W3-的空间构型为_____________。
(3)XTW-的等电子体中属于分子的有_____________(填化学式,写出一种即可),XTW-的电子式为_____________;
(4)R的某种钠盐晶体,其阴离子Mm-(含Q、R、O三种元素)的球棍模型如下图所示:在Mm-中,R原子轨道杂化类型为_____________,m=_____________。(填数字)

(5)T的某种单质的片层与层状结构如图1所示.其中层间距离为xpm,图2为从结构中取出的晶胞,若晶胞的边长为ypm,则T的该种单质的密度为_____________g•cm-3。(1pm=10-12m)

查看答案和解析>>
科目: 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:填空题
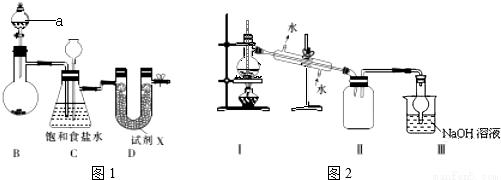
结晶玫瑰和高分子树脂P的合成路线如下图所示:
已知①A的分子式为C7H8
②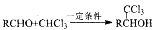
③ (R、R1、R2代表烃基或氢原子)
(R、R1、R2代表烃基或氢原子)
回答下列问题:
(1)C的名称是_____________,E中官能团的名称是____________;
(2)①D→I的反应类型为____________;
②B→C的化学方程式为____________;
(3)由I生成结晶玫瑰的化学方程式为____________;
(4)①在上述流程中“E→F”及“G→H”在P的合成过程中的作用是____________。
②高分子P的结构简式为____________;
(5)已知I在一定条件下水解生成J(C8H8O3),写出满足下列条件的J的同分异构体的结构简式____________。
A.遇三氯化铁溶液显紫色
B.苯环上的一氯取代物只有一种
C.与足量的氢氧化钠溶液反应,1mol该物质可消耗3molNaOH。
查看答案和解析>>
科目: 来源:2016届江苏省高三5月四模化学试卷(解析版) 题型:选择题
化学知识在环境保护中起关键作用,下列叙述不正确的是
A.在燃煤中加入适量的生石灰能有效减少二氧化硫的排放
B.控制含磷洗涤剂的生产和使用有利于防止水体富营养化
C.采用汽车尾气处理技术可将汽车尾气中的NO和CO转化为无害气体
D.使用加酶洗衣粉,水温越高,洗涤效果更好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com