
科目: 来源:2016届黑龙江省高三考前训练二理综化学试卷(解析版) 题型:填空题
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%,二氧化碳(CO2)的排放量也要大幅减少。
(1)在恒温,容积为1 L恒容中,硫可以发生如下转化,其反应过程和能量关系如图1所示(已知:2SO2(g)+O2(g)  2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
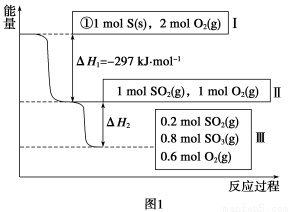
①写出能表示硫的燃烧热的热化学方程式:_________________________________。
②ΔH2=__________kJ·mol-1。
③在相同条件下,充入1 mol SO3和0.5 mol的O2,则达到平衡时SO3的转化率为______________;此时该反应________(填“放出”或“吸收”)________kJ的能量。
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
①CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图2所示。从3 min到9 min,v(H2)=________mol·L-1·min-1。
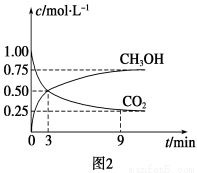
②能说明上述反应达到平衡状态的是________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
③为了加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有________(填编号)。
A.升高温度 B.缩小容器体积 C.再充入CO2气体 D.使用合适的催化剂
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g)  CH3OH(g)的平衡常数。下列说法正确的是________。
CH3OH(g)的平衡常数。下列说法正确的是________。
温度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应ΔS<0
C.在T ℃时,1 L密闭容器中,投入0.1 mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5 MPa)和250 ℃,是因为此条件下,原料气转化率最高
查看答案和解析>>
科目: 来源:2016届黑龙江省高三考前训练二理综化学试卷(解析版) 题型:填空题
可降解聚合物G可由芳香烃A通过如下途径制备,质谱法测定A相对分子质量为102。
已知:①B为高分子化合物,D的化学式为C8H10O2
②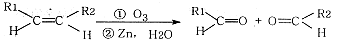
③碳碳双键的碳上连有羟基的有机物不稳定
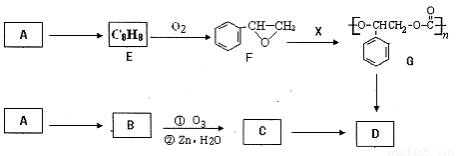
(1)A的化学式为_________,X的化学式为_____________;
(2)写出B的结构简式 。
(3)写出C→D的化学方程式 。
(4)G 在一定条件下水解得到D,写出G→D的化学方程式 。
(5)同时符合下列条件F的稳定同分异构体共 种,写出其中一种结构简式 。
①遇FeCl3不显紫色,除苯环外不含其它环状结构;
②苯环上有三种不同化学环境的氢原子; ③不能发生银镜反应。
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
明·于谦诗:“凿开混沌得乌金,藏蓄阳和意最深。爝火燃回春浩浩,洪炉照破夜沉沉。”这里“乌金”指的是
A.煤 B.磁铁矿 C.石油 D.金
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
莽草酸因可以作为合成达菲(抗病毒和抗癌药)的中间体而受到重视,其结构简式如图,下列关于莽草酸的说法正确的是
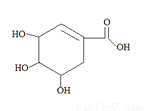
A.分子中含有三种含氧官能团
B.可发生取代、加成及氧化反应
C.在水溶液中羟基和羧基均能电离出氢离子
D.与足量的钠反应能产生44.8L气体
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.c(H+)=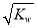 mol·L-1的溶液:Fe3+、K+、Cl-、CO32-
mol·L-1的溶液:Fe3+、K+、Cl-、CO32-
B.c(NH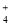 )=0.1mol·L
)=0.1mol·L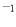 的(NH4)2Fe(SO4)2溶液:H
的(NH4)2Fe(SO4)2溶液:H 、Al
、Al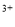 、Br
、Br 、I
、I
C.加水稀释时,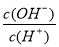 值明显增大的溶液:K+、NH4+、CO32-、MnO4-
值明显增大的溶液:K+、NH4+、CO32-、MnO4-
D.通入SO2的饱和溶液:Ca2+、K+、NO3-、Cl-
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
下列实验操作能达到预期实验目的的是
实验目的 | 实验操作 |
A.证明Fe3+与SO2发生了氧化还原反应 | 将过量SO2通入FeCl3溶液中,然后将反应液加入酸性高锰酸钾溶液中,发现高锰酸钾溶液褪色 |
B.除去CH3COOC2H5中的乙醇 | 加入适量CH3COOH,加热 |
C.比较AgCl和AgI的 Ksp大小 | 向10mL浓度均为0.01mol/L的NaCl和KI混合溶液滴加少量0.01mol/L AgNO3溶液,观察现象 |
D.比较H2CO3、HCN的酸性强弱 | 用pH计测定同温度同浓度的Na2CO3溶液和NaCN溶液的pH值,比较pH大小 |
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
短周期元素W、X、Y和Z的原子序数依次增大。其中W的原子半径最小,X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,且Y和Z可以形成化合物ZY2和ZY3。根据以上叙述,下列说法中正确的是
A.原子半径大小为W<X<Y<Z
B.W与X、Y、Z分别形成最简单化合物中最稳定的是Z
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
锂—铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电能,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是
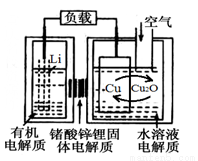
A.放电时,Li+透过固体电解质向Cu极移动
B.放电时,正极的电极反应式为O2+2H2O+4e-=4OH-
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,氧化剂为O2
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:选择题
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.2 | 0.2 | pH=9 |
丙 | c1 | 0.2 | pH =7 |
丁 | 0.2 | 0.1 | pH<7 |
下列判断正确的是
A.c1=0.2 B.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-)
C.a>9 D.在乙组混合液中由水电离出的c(OH-)=10-5mol·L-1
查看答案和解析>>
科目: 来源:2016届山西省等校高三下第四次联考理综化学A卷(解析版) 题型:实验题
钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO3),还含有少量Fe2O3]为原料制备钛的工艺流程如图所示:
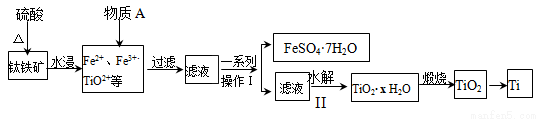
(1)钛铁矿与硫酸反应的化学方程式为 。
(2)加入的物质A为 。
(3)步骤Ⅱ中发生反应的离子方程式为 ;水解过程中需要升高温度,其目的是:①加快反应水解速率 ② 。
(4)由TiO2获得金属Ti可用以下两种方法。
①电解法:以石墨为阳极,TiO2为阴极,熔融CaO为电解质,其阴极的电极反应式为 。
②热还原法:首先将TiO2、氯气和过量焦炭混合,高温反应生成TiCl4;然后用Mg还原TiCl4即可制取Ti。生成TiCl4的反应中,氧化剂与还原剂的物质的量之比为 ;生成Ti的反应需在Ar气氛中,其原因为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com