
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
下列物质变化时,不需要破坏化学键的是( )
A.HCl溶于水 B.烧碱熔化 C.H2燃烧 D.I2升华
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
原子序数依次增大的元素W、X、Y、Z,它们的最外层电子数分别为1、6、7、1。W-的电子层结构与氦相同,X和Y的次外层有8个电子,Y-和Z+的电子层结构相同。下列叙述错误的是( )
A.元素的非金属性次序为Y>X>W
B.W和其他3种元素均能形成共价化合物
C.Z和其他3种元素均能形成离子化合物
D.元素W、X、Y各自最高和最低化合价的代数和分别为0、4、6
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素中,气态氢化物稳定性最好的其单质氧化性也最强
C.同周期非金属氧化物对应水化物的酸性从左到右依次增强
D.第二周期元素的最高化合价为+1→+7
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
有M、R两种主族元素,已知M2-与R+核外电子数之和为20,则下列不正确的是( )
A.M与R的质子数之和一定等于19
B.M、R可能分别处于第二周期和第三周期
C.M、R可能分别处于第三周期和第二周期
D.M和R的质子数之差可能等于7
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
依据下表短周期元素原子半径及主要化合价,下列叙述正确的是( )
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.还原性H2T>H2R
B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物能与NaOH溶液反应
D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10L密闭容器中进行,30s后,水蒸气的物质的量增加了4.5mol,则此反应的平均速率v(X)可表示为( )
4NO(g)+6H2O(g)在10L密闭容器中进行,30s后,水蒸气的物质的量增加了4.5mol,则此反应的平均速率v(X)可表示为( )
A.v(NH3)=0.010mol.L-1.s-1 B.v(O2)=0.010mol.L-1.s-1
C.v(NO)=0.15mol.L-1.s-1 D.v(H2O)=0.15mol.L-1.s-1
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分,回答相关的问题
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑾ |
(1)写出④的元素符号;
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式______________。
(3)在这些元素中,最高价氧化物的水化物酸性最强的是______________ (填相应化学式,下同),碱性最强的是______________。
(4)这些元素中(除⑨外),原子半径最小的是______________ (填元素符号,下同),原子半径最大的是______________。
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为______________ (方程式中用具体元素符号表示)。
(6)⑦的低价氧化物通入足量Ba(NO3)2溶液中的离子方程式______________。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:实验题
常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)?
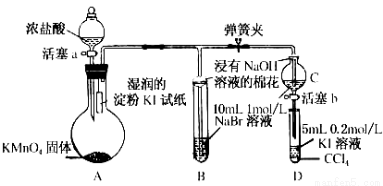
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸?
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹?
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a?
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是___________________?
(2)验证氯气的氧化性强于碘的实验现象是______________?
(3)B中溶液发生反应的离子方程式是______________?
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是______________。
(5)过程Ⅲ实验的目的是______________?
(6)氯?溴?碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,电子层数依次增多,______________,得电子能力逐渐减弱,非金属性逐渐减弱?
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:填空题
W、X、Y、Z是原子序数依次增大的同一短周期主族元素,W、X是金属元素,Y、Z是非金属元素。W、X两者的最高价氧化物对应的水化物可以起反应生成盐和水。
(1)W的名称是______________,上述反应的离子方程式为______________。
(2)W与Y可形成化合物W2Y,Y的离子结构示意图为______________,该化合物的电子式为______________。
(3)X与Z可形成化合物是共价化合物而不是离子化合物,设计一个实验证明之:______________。
(4)Y的低价氧化物和Z的单质在水溶液中反应的化学方程式是:______________。
(5)Y与Z能形成一种化合物,其所有原子都满足8电子结构,其分子式为______________。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:填空题
人们应用原电池原理制作了多种电池以满足不同的需要。电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl
①该电池的负极反应式是______________;
②在电池中,Na+不断移动到“水”电池的_______极(填“正”或“负”);
③外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是______________。
(2)中国科学院应用化学研究所在甲醇(CH3OH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃料电池的工作原理如右图所示。
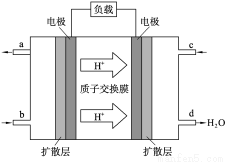
①该电池工作时,b口通入的物质为______________。
②该电池负极的电极反应式______________。
③工作一段时间后,当6.4g甲醇完全反应生成CO2时,有___________NA个电子转移。
(3)Ag2O2是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com