
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:选择题
将标准状况下V mL CO2缓慢通入200 mL 0.15mol/L的NaOH溶液中,气体被充分吸收,下列关系不正确的是( )
A.V=336 mL时,c(OH-) = c(H+) +c(HCO3-)+2c(H2CO3)
B.V=448 mL时,2c(Na+)=3[c(H2CO3)+c(HCO3-)+c(CO32-)]
C.V=672 mL时,c(Na+) >c(HCO3-)> c(OH-)> c(CO32-) >c(H+)
D.通入CO2过程中恒有关系式:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:选择题
对于下列四幅图象的表述正确的是
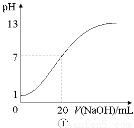

A.图①表示25℃时,用0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1 盐酸溶液,溶液的pH随加入NaOH溶液体积的变化
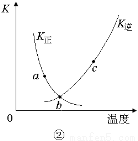
B.图②中表示反应2SO2(g) + O2(g)  2SO3(g);ΔH<0的有关曲线,图中A.B.c三点中只有b点已经达到化学平衡状态.
2SO3(g);ΔH<0的有关曲线,图中A.B.c三点中只有b点已经达到化学平衡状态.
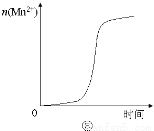
C.图③表示10 mL 0.01 mol·L-1KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4 溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用)
D.图④中a、b曲线分别表示反应CH3CH3→CH2=CH2 (g) + H2(g);ΔH>0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:实验题
甲、乙两池电极材料都是铁棒与碳棒(如图)。请回答下列问题:
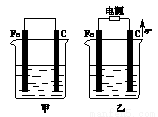
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的______棒;乙池中的______棒。
②在乙池中阳极的电极反应是______________________________。
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中总反应的离子方程式:
_______________________________________________________________________。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去。这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸。该反应的化学方程式为___________________________________________________________。
(3)如下图为相互串联的甲、乙两个电解池(电极都是惰性电极),请回答:
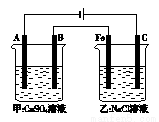
①写出甲电解池中的电解反应方程式:_______________________________________________。
②若甲槽阴极增重12.8 g,则乙槽阳极放出气体在标准状况下的体积为___________;若乙槽剩余液体为400 mL,则电解后得到碱液的物质的量浓度为______________。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
(1)对金属制品进行抗腐蚀处理,可延长其使用寿命。
以下为铝材表面处理的一种方法
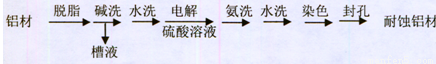
①碱洗的目的是洗去铝材表面的自然氧化膜,碱洗时常有气泡冒出,其原因是_________________
__________________________________ (用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 ______。
A.NH3 B.CO2 c.NaOH D.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,
阳极的电极反应式为 ____________ 。电解后的铝材需氨洗的目的是_____________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是____________________
____________________________________________________________________。
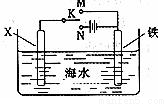
(3)利用下图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应该置于 处。若X为锌,开关K置于M处,该电化学防护法称为 _________________。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为
__________________________________________________________________________。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
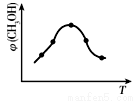
取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如右图所示,则上述CO2转化为甲醇的反应热△H3_____0(填“>”、“<”或“=”),该反应的平衡常数表达式为______________________________________________________。
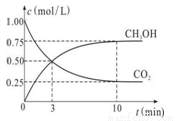
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如右图所示。试回答:0~10 min内,氢气的平均反应速率为_________mol/(L·min)。第10 min后,若向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数_________(填“变大”、“减少”或“不变”)。
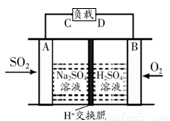
(3)脱硫。①有学者想利用如右图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。则电子流出的电极为_____(用A或B表示),A极的电极反应式为______________________________。
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,其原因用离子方程式表示为_________________________;常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液中的NO3-和NH4+的物质的量浓度相等,则溶液的pH_____7(填写“>”“=”或“<”)。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
学习选修5的学生必做题
(1)由两种烃组成的混合气体2L与足量的氧气充分反应后生成CO2 5L、H2O 7L(所有体积都在120℃测定),则这两种混合气体的可能组成是( )
A.C2H4、C3H8 B.CH4、C5H8 C.CH4、C4H8 D.C2H6、C3H8
(2)下列变化中,由加成反应引起的是( )
A.乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B.苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷
C.一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成
D.由电石制乙炔
(3)下列说法正确的是( )
甲苯的一氯代物有4种,将甲苯加氢饱和后的产物的一氯代物也有4种
B.所有汽油都可以用于萃取溴水中的溴
C.通过核磁共振氢谱图可以知道有机物的空间等效氢原子种类和数目
D.分子式为C6H12的烯烃,主链上有四个碳原子的同分异构体只有4种
(4)以煤为原料制备一些化工产品的前景被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。

请回答下列问题:
①反应①反应类型________________E中官能团名称__________。
②写出结构简式:PVC_________________C_____________________。
③写出反应③的化学方程式:_____________________________________________。
④写出A D的化学反应方程式___________________________________________。
D的化学反应方程式___________________________________________。
查看答案和解析>>
科目: 来源:2015-2016学年四川省高二4月月考化学试卷(解析版) 题型:填空题
未学习选修5的学生必做题
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示: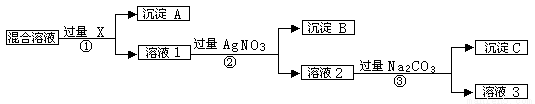
请回答下列问题:
⑴试剂X的电子式__________________________,沉淀A的晶体类型__________________________,
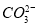 的空间构型是__________________________。
的空间构型是__________________________。
⑵上述实验流程中加入过量的Na2CO3的目的是___________________________________。
发生反应的离子方程式是:_____________________________________________________。
⑶按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________,之后若要获得固体NaNO3需进行的实验操作是___________(填操作名称)。
查看答案和解析>>
科目: 来源:2015-2016学年福建省高一下学期期中化学试卷(解析版) 题型:选择题
Si、SiO2广泛用于制造晶体管、光导纤维等,下列有关说法正确的是( )
A.附着油污的晶体管可用碱液浸泡
B.光导纤维遇碱会影响光信号传输
C.工业上用S iO2热分解法冶炼硅
D.自然界中硅以游离态形式存在
查看答案和解析>>
科目: 来源:2015-2016学年福建省高一下学期期中化学试卷(解析版) 题型:选择题
下列说法中,正确的是( )
A.任何化学反应都伴随着能量的变化
B.H2O(气)―→H2O(液)该过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.所有的物质一定存在化学键
查看答案和解析>>
科目: 来源:2015-2016学年福建省高一下学期期中化学试卷(解析版) 题型:选择题
用氯化铝制取纯净的硝酸铝的最佳方法是 ( )
A.用氯化铝和纯硝酸反应
B.氯化铝与氢氧化钠反应,过滤得沉淀,再加稀HNO3
C.用AlCl3溶液和氨水反应,过滤得沉淀,再加稀HNO3
D.AlCl3溶液和Ba(NO3)2溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com