
科目: 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:填空题
A、B、C、D、E五种元素都是前36号元素,原子序数依次增大,其相关信息如下表:
元素 | 相关信息 |
A | A的第一电离能低于同周期左右相邻元素 |
B | B原子中成对电子数等于未成对电子数的2倍 |
C | C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 |
D | D与A、B、C均不同周期,其一个单质分子中只有一个σ键 |
E | E的原子序数比所处周期中未成对电子数最多的元素大3 |
(1)写出上述一种元素与氢元素形成的X2Y2型非极性分子的结构式:________。
(2)写出E元素的元素符号:________,其价电子排布图为:________。
(3)A与D形成化合物的化学式为________,是________分子(填“极性”或“非极性”)
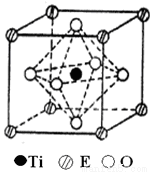
(4)在ETiO3晶胞中(结构如图2所示),1个Ti原子和1个E原子周围距离最近的O原子数目分别为________个、________个.
(5)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-.N3-的空间构型为________,叠氮化物能与E3+形成配合物,则[E(N3)(NH3)5]SO4中配体是________,E的配位数是________。
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
化学是你,化学是我,化学深入我们生活,下列有关说法不正确的是( )
A.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
B.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列说法正确的是( )
A.3.1g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA
B.0.1mol丙烯醛中含有双键的数目为0.1NA
C.标准状况下,2.24L乙醇中含有的分子数目为0.1NA
D.1molNaHSO4固体中阳离子的数目为2NA
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
2015年,中国科学家屠呦呦因发现治疗疟疾的药物青蒿素获得了诺贝尔奖。青蒿素的结构如图所示,下列有关青蒿素的说法中正确的是( )
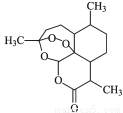
A.分子式为C15H20O5
B.具有较强的还原性
C.易溶于水,乙醇和乙醚
D.氧原子的化合价有-1和-2
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
W、X、Y、Z均为短周期主族元素,原子序数依次增加,X与Y形成的化合物能与水反应生成酸且X、Y同主族,两元素核电荷数之和与W、Z的原子序数之和相等,则下列说法正确的是( )
A.Z元素的含氧酸一定是强酸
B.原子半径:X>Z
C.气态氢化物热稳定性:W>X
D.W、X与H形成化合物的水溶液可能呈碱性
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
下列实验方案设计不合理的是
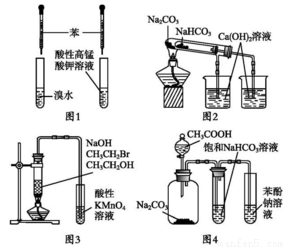
A.图1:验证苯中是否有碳碳双键
B.图2:验证NaHCO3和Na2CO3的热稳定性
C.图3:验证溴乙烷发生消去反应生成烯烃
D.图4:验证酸性CH3COOH>H2CO3>C6H5OH
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
一种酸性“二甲醚(CH3OCH3)直接燃料电池”具有启动快、能量密度高、效率好等优点,其电池原理如图所示.下列有关该电池的说法不正确的是( )
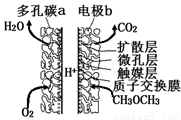
A.多孔碳a能增大气固接触面积,提高反应速率,该电极为负极
B.电极b上发生的反应为:CH3OCH3-12e-+3H2O═2CO2+12H+
C.H+由b电极向a电极迁移
D.二甲醚直接燃料电池能量密度(kW•h•kg-1)约为甲醇(CH3OH)直接燃料电池能量密度的1.4倍(单位质量二甲醚和甲醇所释放电能)
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列说法中正确的是
A.该现象说明了NaHCO3难溶于水
B.滤液中的c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.滤液中c(Na+)+c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+c(CO32-)
D.滤液中c(Cl-)>c(NH4+)> c(HCO3-)> c(H+)>c(OH-)
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:填空题
某实验小组欲制取氯酸钾,并测定其纯度。制取装置如图甲所示。请回答:
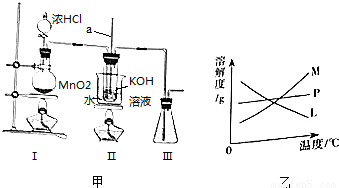
(1)Ⅱ中玻璃管a的作用为__________。
(2)为了提高KOH的利用率,可将上述实验装置进行适当改进,其方法是__________。
(3)反应完毕经冷却后,Ⅱ的大试管中有大量KClO3晶体析出.图乙中符合该晶体溶解度曲线的是__________(填编号字母);要从Ⅱ的大试管中分离已析出晶体,下列仪器中不需要的是__________(填仪器编号字母)。
A.铁架台 B.长颈漏斗 C.烧杯 D.蒸发皿 E.玻璃棒 F.酒精灯
(4)上述制得的晶体中含少量KClO、KCl杂质.
已知:碱性条件下,ClO-有强氧化性,ClO3-很稳定;酸性条件下,ClO-、ClO3-都具有较强的氧化性.
为测定KClO3的纯度,进行如下实验:
步骤1:去上述晶体3.00g,溶于水配成100mL溶液.
步骤2:取20.00mL溶液于锥形瓶中,调至pH=10,滴加双氧水至不再产生气泡,煮沸.
步骤3:冷却后,加入足量KI溶液,再逐渐滴加入足量稀硫酸.
发生反应:ClO3-+I-+H+→Cl++I2+H2O(未配平)
步骤4:加入指示剂,用0.5000mol•L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液48.00mL,发生反应:2S2O32-+I2═S4O62-+2I-.
①步骤2中用双氧水除去溶液中残留ClO-的离子方程式为__________。
②该晶体中KClO3的质量分数为__________。
③若步骤2中未进行煮沸,则所测KClO3的质量分数__________(填“偏低”、“偏高”或“无影响”)
查看答案和解析>>
科目: 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料,又可称为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-58kJ·mol-1
③CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ·mol-1
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O |
| H-O | C-H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | x |
则x=__________。
(2)若T℃时将6molCO2和 8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间的变化如图中状态Ⅰ(图中实线)所示。图中数据A(1,6)代表在1min时H2的物质的量是6mol。
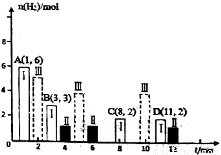
①T℃时状态I条件下,0--3min内CH3OH的平均反应速率v=__________(保留两位有效数字),
平衡常数K=__________;
②其他条件不变时,仅改变某一条件后测得H2的物质的量随时间变化如图中状态Ⅱ所示,则改变的条件可能是__________。
③一定温度下,此反应在恒容容器中进行,能判断该反应达到化学平衡状态依据的是__________
a.容器中压强不变
b. CO2和水蒸气的体积比保持不变
c. v正(H2) =3v逆(CH3OH )
d.气体的密度不再随时间的改变而变化
④CO与H2在密闭容器中发生反应①,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示。下列说法正确的是__________
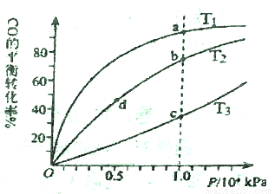
A.温度:T1<T2<T3
B.正反应速率:v(a)>v(c);v(b)>v(d)
C.平衡常数:K(a)>K(c);K(b)>K(d)
D.平均摩尔质量:M(a)<M(c);M(b)>M(d)
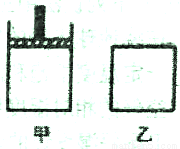
⑤800K向下列起始体积相同的密闭容器中充入1molCO、2molH2发生反应①,如图所示甲容器在反应过程中保持压强不变,乙容器保持体积不变达到平衡时H2的浓度c (H2)甲__________c(H2)乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com