
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
下列判断正确的是( )
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C.晶体中一定存在化学键
D.正四面体分子中键角可能是109°28′或60°
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。下列说法正确的是( )
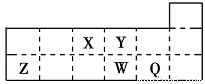
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ。
C.Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的外围电子排布图为:
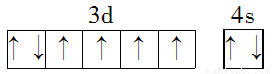
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
下列有关说法不正确的是( )
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、N2都是非极性分子
C.酸性:H2CO3<H3PO4<H2SO4<HClO
D.CO的一种等电子体为NO+,它的电子式为[:N??O:]+
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
在有机物中,若碳原子上连接的四个原子或原子团不相同,则这个碳原子称为手性碳原子。含有手性碳原子的分子一般是手性分子具有镜像异构及光学活性,下列分子中具有光学活性的是( )
A.CBr2F2 B.CH3CH2OH C.CH3CH2CH3 D.CH3CH(OH)COOH
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
填写下列空白
(1)第三周期原子半径最小的元素__________。
(2)含有8个质子,10个中子的原子的化学符号__________。
(3)最外层电子排布为4s24p1的原子的核电荷数为__________。
(4)周期表中最活泼的非金属元素价电子排布图为__________。
(5)下列物质中,只含有极性键的分子是 ,既含离子键又含共价键的化合物是 ;只存在σ键的分子是 ,同时存在σ键和π键的分子是 。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为________。
(2)B的氢化物的分子空间构型是________;其中心原子采取________杂化。
(3)一种由B、C组成的化合物与AC2互为等电子体,其化学式为________。
(4)ECl3形成的配合物的化学式为________。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是______________________________________。
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的外围电子排布式为___________________。
(2)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________;1 mol B2A2分子中含________mol σ键。
(3)已知D、E能形成晶胞结构如图所示的两种化合物,则化学式:甲为____________________,乙为______________________;高温时,甲易转化为乙的原因为_____________________________。
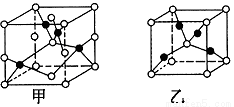
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素原子最外层的p轨道中的电子数等于前一电子层的电子总数,X原子最外层的p轨道中有一个轨道填充了2个电子。
(1)X原子的电子排布式是____________,Y原子的价层电子排布图是: 。
(2)YX2的立体构型是________,YX2的熔、沸点比ZX2________(填“高”或“低”)。
(3)YX2分子中,Y原子的杂化类型是________,一个YX2分子中含________个π键。
(4)下图表示一些晶体的结构(晶胞),其中代表YX2的是________,代表ZX2的是________(填序号,下同)。
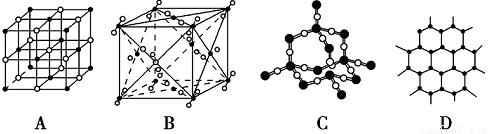
查看答案和解析>>
科目: 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N的电负性由大到小的顺序是 。C60和金刚石都是碳的同素异形体,二者比较,熔点高的是 。
(2)A、B均为短周期金属元素,依据下表数据,写出B的基态原子的电子排布式 
过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色。据此判断,
[Mn(H2O)6]2+ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①每个COCl2分子内含有 个σ键, 个π键。其中心原子采取 杂化轨道方式。
②配合物Fe(CO)5的配体是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com