
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:推断题
短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+电子层结构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体,回答下列问题:
(1)M元素位于周期表中的第______周期、_______族。
(2)Z元素是____,其在自然界中常见的二元化合物是____。
(3)X与M的单质在高温下反应的化学方程式为______,产物分子为直线形,其化学键属__________共价键(填“极性”或“非极性”)。
(4)四种元素中的____可用于航空航天合金材料的制备,其单质与稀盐酸反应的化学方程式为_________。
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:实验题
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:

(1)为尽量少引入杂质,试剂①应选用___(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3 AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:推断题
乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成。回答下列问题:

(1)B和A为同系物,B的结构简式为_______。
(2)反应①的化学方程式为___________,其反应类型为__________。
(3)反应③的反应类型为____________。
(4)C的结构简式为___________。
(5)反应②的化学方程式为______。
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:填空题
顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化:
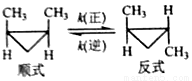
该反应的速率方程可表示为:v(正)=k(正)c(顺)和v(逆)=k(逆)c(反),k(正)和k(逆)在一定温度时为常数,分别称作正,逆反应速率常数。回答下列问题:
(1)已知:t1温度下,k(正)=0.006s-1,k(逆)=0.002s-1,该温度下反应的平衡常数值K1=_____;该反应的活化能Ea(正)小于Ea(逆),则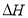 ________0(填“小于”“等于”或“大于”)。
________0(填“小于”“等于”或“大于”)。
(2)t2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_______(填曲线编号),平衡常数值K2=_____;温度t2___t1(填“小于”“等于”或“大于”),判断理由是______。

查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:实验题
某废催化剂含58.2%的SiO2、21.0%的ZnO、4.5%的ZnS和12.8%的CuS。某同学用15.0 g该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下:
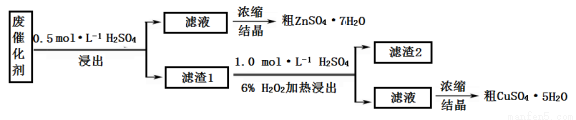
回答下列问题:
(1)在下列装置中,第一次浸出必须用____________,第二次浸出应选用____________。(填标号)
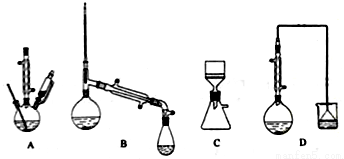
(2)第二次浸出时,向盛有滤液1的反应器中加入稀硫酸,后滴入过氧化氢溶液。若顺序相反,会造成___________。滤渣2的主要成分是____________________。
(3)浓缩硫酸锌、硫酸铜溶液使用的器皿名称是________________。
(4)某同学在实验完成之后,得到1.5gCuSO4﹒5H2O,则铜的回收率为__________________。
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:选择题
下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为2?1的有
A. 乙酸甲酯 B. 对苯二酚 C. 2-甲基丙烷 D. 对苯二甲酸
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:推断题
富马酸(反式丁烯二酸)与Fe2+形成的配合物——富马酸铁又称“富血铁”,可用于治疗缺铁性贫血。以下是合成富马酸铁的一种工艺路线:
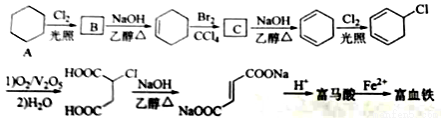
回答下列问题:
(1)A的化学名称为_____;由A生成B的反应类型为_____。
(2)C的结构简式为_____。
(3)富马酸的结构简式为_____。
(4)检验富血铁中是否含有Fe3+的实验操作步骤是_____。
(5)富马酸为二元羧酸,1mol富马酸与足量饱和NaHCO3溶液反应可放出____L CO2(标况);富马酸的同分异构体中,同为二元羧酸的还有____________(写出结构简式)。
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:选择题
下列叙述正确的有
A. 第四周期元素中,锰原子价电子层中未成对电子数最多
B. 第二周期主族元素的原子半径随核电荷数增大依次减小
C. 卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:填空题
M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为______,晶体中原子间通过_____作用形成面心立方密堆积,其中M原子的配位数为______。
(2)元素Y基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。
(3)M与Y形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为_______,已知晶胞参数a=0.542 nm,此晶体的密度为_______g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______。
查看答案和解析>>
科目: 来源:2016年全国普通高等学校招生统一考试化学(海南卷精编版) 题型:填空题
Ⅰ下列单元操作中采用了热交换设计的有
A.电解食盐水制烧碱
B.合成氨中的催化合成
C.硫酸生产中的催化氧化
D.氨碱法中的氨盐水碳酸化
Ⅱ海水晒盐的卤水中还有氯化镁,以卤水为原料生产镁的一中工艺流程如下图所示。
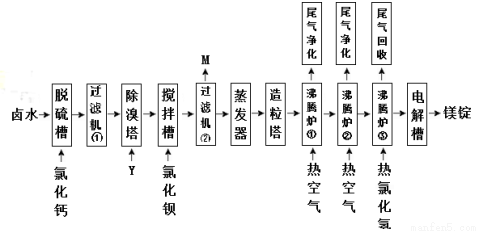
回答下列问题:
(1)脱硫槽、搅拌槽均用于脱除卤水中的(填离子符号),M的主要成分是(填化学式)。
(2)除溴塔中主要的离子方程式为。
(3)沸腾炉①和②的主要作用是。沸腾炉③通入热氯化氢的主要目的是。
(4)电解槽中阴极的电极反应方程式为。
(5)电解槽中阳极产物为,该产物可直接用于本工艺流程中的。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com