
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
苹果酸的结构简式为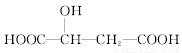 ,下列说法正确的是
,下列说法正确的是
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成1 mol H2
D. 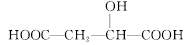 与苹果酸互为同分异构体
与苹果酸互为同分异构体
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图所示(未表示出原子或原子团的空间排列)。该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是

A.Br2的CCl4溶液 B.Ag(NH3)2OH溶液
C.HBr D.H2
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如右图所示。下列说法正确的是
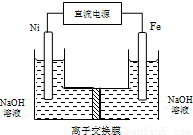
A.铁是阳极,电极反应为Fe-2e-+2OH-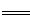 Fe(OH)2
Fe(OH)2
B.电解一段时间后,镍电极附近溶液的pH减小
C.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
D.每制得1mol Na2FeO4,理论上可以产生67.2L气体
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
化学与生产、生活息息相关,下列叙述正确的是
A.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
B.用聚乳酸塑料代替聚乙烯塑料能减少白色污染
C.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如下图所示,该电池的电解质为6 mol·L-1KOH溶液,下列说法中正确的是
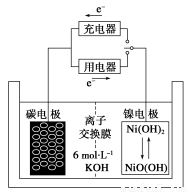
A.放电时K+移向负极
B.放电时电池负极的电极反应为H2-2e-===2H+
C.放电时电池正极的电极反应为NiO(OH)+H2O+e-===Ni(OH)2+OH-
D.该电池充电时将碳电极与电源的正极相连
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应: X(g)+Y(g) 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z,建立平衡状态I,此时Y的体积分数为w%。下列说法正确的是( )
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z,建立平衡状态I,此时Y的体积分数为w%。下列说法正确的是( )
A.用V(X)和V(Y)表示此反应的反应速率是:V(X)=V(Y)=(0.1-0.2a)mol·(L·min)-1
B.当混合气体的质量不再发生变化时,说明反应达到平衡状态,此时气体总量为(1+n)mol
C.若建立平衡I的起始时n=1,维持温度和体积不变,向平衡I的体系中再加入cmolZ和dmolM
[其中c>0的任意值,d≥(1-a)mol],达到平衡状态II,此时Y的体积分数一定为w%
D.维持温度和体积不变,向上述平衡体系中再充入l mol X和n mol Y,此时v(正)增大,v(逆)减小,平衡正向移动,再次达到平衡时,Z的物质的量浓度为2a mol/L,M的物质的量为2a mol
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
在恒容密闭容器中通入X并发生反应:2X(g)  Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是

A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= mol·L-1·min-1
mol·L-1·min-1
C.M点的正反应速率v正大于N点的逆反应速率v逆
D.M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:简答题
暗紫色化合物A具有绿色、高电压和高能量的特点,近年来引起了电化学界的高度重视。在常温和干燥的条件下,化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质。某兴趣小组的同学对化合物A进行组成分析,确定A中仅含有O、K、Fe三种元素。取3.96g化合物A的粉末溶于水,滴加足量的稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)化合物A的化学式为 ;化合物A与H2O反应的离子方程式为 。
(2)化合物A还可作为一种“绿色高效多功能”水处理剂。原因是 。
(3)化合物A的制备还可通过氧化法,试写出在KOH存在条件下用次氯酸钾氧化氢氧化铁制备A的化学方程式 。
(4)目前,人们针对化合物A的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高化合物A水溶液稳定性的是
A.亚硫酸钠 B.KOH C.醋酸 D.Fe(NO3)3
(5)为研究温度对化合物A水溶液稳定性的影响,请设计一个实验方案 。
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:简答题
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 ,氧化性最弱的简单阳离子是 。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是 ;
制铝时,电解Al2O3而不电解AlCl3的原因是 。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
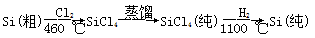
写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
(7)工业上,通过如下转化可制得KClO3晶体: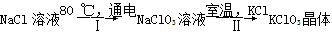
完成Ⅰ中反应的总化学方程式:
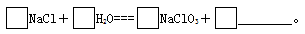
Ⅱ该反应过程能析出KClO3晶体而无其他晶体析出的原因是 。
查看答案和解析>>
科目: 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:推断题
烃的含氧衍生物A,能发生如下图所示的变化。在同温同压下,A蒸气的密度是H2密度的45倍,其中氧元素的质量分数为53.3%; C能使溴的四氯化碳溶液褪色,C在一定条件下转化为高分子化合物D, A中不含甲基,B不属于醚类。
已知: CH3CH2OH→CH2=CH2 + H2O

请填写下列空白:
(1)A的结构简式 C分子中的官能团名称 。
(2)C→D的反应类型是 。A→B的反应类型是 。
(3)A转化为B的化学方程式是 。
(4)3.6克A物质与足量金属钠反应生成的气体在标况的体积 升 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com