
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
图是氢氧燃料电池驱动LED发光的装置.下列有关叙述正确的是
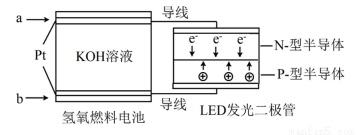
A.氢氧燃料电池中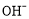 向b极移动
向b极移动
B.该装置中只涉及两种形式的能量转化
C.电池正极电极反应式为O2+2H2O+4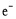 =
=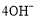
D.P一 型半导体连接的是电池负极
型半导体连接的是电池负极
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对应的装置合理,操作规范的是
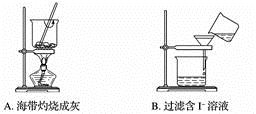

查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
下列实验方案能达到实验目的的是
选项 | 实验方案 | 实验目的或结论 |
A | 将盐酸酸化的双氧水滴入Fe(NO3)2溶液中,溶液变黄色 | H2O2的氧化性比Fe3+强 |
B | 将一小块钠分别投入盛有水和乙醇的小烧杯中,钠与乙醇反应要平缓得多 | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
C | 将某气体通入品红溶液,溶液褪色 | 气体中一定有SO2 |
D | 将铁棒和铜棒用导线连接后放入浓硝酸中,铜棒变细 | 铜的金属性强于铁 |
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
被称为“软电池”的纸质电池,采用一个薄层纸片(在其一边镀锌,在其另一边镀二氧化锰)作为传导体.在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为Zn+2MnO2+H2O═ZnO+2MnO(OH),下列说法正确的是
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当0.1 mol Zn完全溶解时,流经电解液的电子个数为1.204×1023
D.电池正极反应式为MnO2+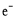 +H2O═MnO(OH)+
+H2O═MnO(OH)+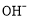
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
根据表中八种短周期元素的有关信息判断,下列说法错误的是
元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
A.元素②⑥形成的化合物具有两性
B.元素②氢化物的沸点小于元素⑤氢化物的沸点
C.元素⑤对应的离子半径大于元素⑦对应的离子半径
D.元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
在标准状况下,由甲烷、甲醛(HCHO)和乙烷组 成的11.2升的混合气体完全燃烧后,生成0.7mol的二氧化碳气体。则混合气体中乙烷的体积分数为
成的11.2升的混合气体完全燃烧后,生成0.7mol的二氧化碳气体。则混合气体中乙烷的体积分数为
A.20% B.40% C.60% D.80%
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:填空题
近年来,国际原油价格大幅上涨,促使各国政府加大生物能源生产,其中乙醇汽油已进入实用化阶段。
(1) 乙醇官能团的电子式为____________;
(2)乙醇在铜或银做催化剂的条件下,可以被空气中的氧气氧化成X,该反应的化学方程式是 ;
(3)乙醇可以被直接氧化成Y(Mr=60),需要加入的试剂是_____________________;在浓硫酸作用下,乙醇与Y反应可生成一种有香味的 物质W,该反应的类型为_____________________;
物质W,该反应的类型为_____________________;
(4)现有两瓶无色液体,分别盛有Y、W,只用一种试剂就可以鉴别,该试剂可以是__________;
A.水
B.乙醇
C.紫色石蕊试液
D.苯
E.碳酸钠溶液
(5)工业上通过乙烯与水在一定条件下反应制得乙醇,反应类型是________,现代石油化工采用银做催化剂,乙烯能被氧气氧化生成M。该反应的原子利用率为100%,反应的化学方程式为 ;
(6)乙醇-氧气燃料电池是以KOH溶液作为电解质溶液,写出其负极的电极反应式___________。
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:填空题
腈纶织物广泛地用作衣物、床上用品等。腈纶是由CH2=CH-CN聚合而成的,CH2=CH-CN可以由下列反应制得:□CH3-CH=CH2+□NH3+□O2→□CH2=CH-CN+□H2O
丙烯可以由石脑油裂解制得:C10H22→2C3H6+X
(1)配平方程式:□CH3-CH=CH2+□NH3+□O 2→□CH2=CH-CN+□H2O
2→□CH2=CH-CN+□H2O
(2)写出上述反应式中X的同分异构体的结构简式 ;
(3)生物质含有葡萄糖、淀粉和纤维素等糖类,也称碳水化合物,绿色植物将二氧化碳和水变成碳水化合物,写出由二氧化碳和水变成葡萄糖的化学方程式 ;
(4)葡萄糖在碱性、加热条件下,能与 (试剂名称)反应析出光亮的金属;在加热条件下,也可与新制的氢氧化铜反应,写出该反应现象 。
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:填空题
为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如表,t表示收集a mL O2所需的时间:
序号 | 反应 温度/℃ | c(H2O2)/ mol•L﹣1 | V(H2O2) /mL | m(MnO2) /g | t/min | |||||||
1 | 20 | 2 | 10 | 0 | t1 | |||||||
2 | 20 | 2 | 10 | 0.1 | t2 | |||||||
3 | 20 | 4 | 10 | 0.1 | t3 | |||||||
4 | 40 | 2 | 10 | 0.1 | t4 | |||||||
(1)设计实验2和实验3的目的是研究 对化学反应速率的影响;
(2)为研究温度对化学反应速率的影响,可以将实验 和实验 作对比(填序号);
(3)将实验1和实验2作对比,t1 t2(填“>”、“<”或“=”)。
Ⅱ.以KI和FeCl3反应为例(2Fe3++2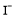 ?2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
?2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
①0.1mol•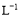 KI溶液
KI溶液
②0.1mol•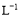 FeCl3溶液
FeCl3溶液
③0.1mol•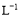 FeCl2溶液
FeCl2溶液
④0.1mol•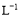 盐酸
盐酸
⑤0.1mol•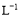 KSCN溶液
KSCN溶液
⑥CCl4
实验步骤:(1)取5mL 0.1mol•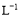 KI溶液,再滴加几滴0.1mol•
KI溶液,再滴加几滴0.1mol•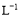 FeCl3溶液;
FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂 (填序号),现象 ,说明此反应存在一定的限度。
Ⅲ.N2O4可分解为NO2。在100mL密闭容器中投入0.01mol N2O4,利用现代化学实验技术跟踪测量c(NO2)。c(NO2)随时间变化的数据记录如图所示:
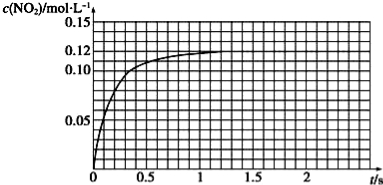
(1)反应容器中最后剩余的物质有 ,其中N2O4的物质的量为 mol;
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小 ,最后 。(选填“变大”,“变小”或“不变”)
,最后 。(选填“变大”,“变小”或“不变”)
查看答案和解析>>
科目: 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:实验题
实验室制备硝基苯的反应原理和实验装置如下:
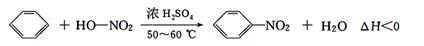
存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯,有关数据如表:
物质 | 熔点/℃ | 沸点/℃ | 密度/ g·cm-3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 |
| 83 | 1.4 | 易溶于水 |
浓硫酸 |
| 338 | 1.84 | 易溶于水 |
实验步骤如下:
取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把17.73 mL(15.6 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60 ℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~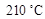 馏分,得到纯硝酸基苯18.45 g。回答下列问题:
馏分,得到纯硝酸基苯18.45 g。回答下列问题:
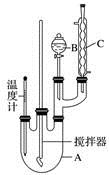
(1)装置B的名称是________,装置C的作用是____________________;
(2)配制混合液时,________(填“能”或“不能”)将浓硝酸加入到浓硫酸中,说明理由:________________________________________________________________________;
(3)为了使反应在50~60 ℃下进行,常用的方法是____________;
(4)在洗涤操作中,第二次水洗的作用是______________________________________;
(5)本实验所得到的硝基苯产率是_________________(保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com