
科目: 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
据此回答以下问题:
(1)①该反应的化学平衡常数表达式为K=________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越________。
(2)某温度下,若把1 mol N2与3 mol H2置于体积为1L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为1/3,则该温度下反应的K的计算式=________(用分数表示)。能说明该反应达到化学平衡状态的是________(填字母)。
a.容器内的密度保持不变
b.容器内压强保持不变
c.v正(N2)=2v逆(NH3)
d.混合气体中c(NH3)不变
(3)对于合成氨反应而言,下列有关图像一定正确的是(选填序号)________。
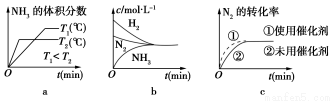
(4)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a________b(填“>”、“=”或“<”,下同),Q1________Q2,Q1________92.4。
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响
用pH计测定25 ℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度/(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)写出醋酸的电离方程式:___________________________________________。
(2)醋酸溶液中存在的微粒有________________________________________。
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是________________________________________________________________________。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将(填“增大”、“减小”或“不变”)__________。
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
请仔细观察下列五种装置的构造示意图,完成下列问题。
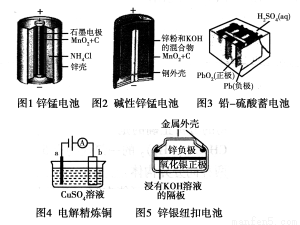
(1)锌锰电池存在自放电现象,主要原因是锌与NH4Cl反应,请结合离子方程式与文字说明原因:
。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2,则负极的电极反应式:________________。
(3)铅-硫酸蓄电池放电的总反应式:Pb+PbO2+2H2SO4=2PbSO4+2H2O,充电过程中,阳极附近c(SO42-)浓度将________(填“变大”、“变小”或“不变”),充电时阴极的电极反应式为:________________。
(4)电解精炼铜时,a极是________(填“纯铜”或“粗铜”)。锌银纽扣电池在工作过程中________(填物质名称)被还原。
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为:________________________。
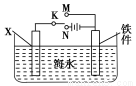
(2)利用右图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________处。
②若X为锌,开关K置于M处,该电化学防护法称为________。
(3)上图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量________3.2 g(填“<”“>”或“=”)。
(4)上图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是 ,若将开关K置于N处,发生的总反应是 。
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
25 ℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17。
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1 L溶液表示)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:__________________。
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)________(填“增大”、“减小”或“不变”)。
(3)X-、Y-、Z-均为0.01mol/L的混合溶液中,逐滴加入AgNO3溶液,产生沉淀的先后顺序是________。
(4)向含有X-、Y-均为0.01mol/L的混合溶液中加入AgNO3溶液,当溶液中Y-沉淀完全时,溶液中Ag+的浓度至少为 mol/L,此时,X- (填是或否)开始沉淀,请结合计算来说明理由: 。
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高一下学期期中化学试卷(解析版) 题型:选择题
关于元素周期表的叙述中不正确的是( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B. 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素
C. 在元素周期表的右上角可以寻找制备新型农药的元素
D. 在地球上元素的分布和它们在元素周期表中的位置有密切关系
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高一下学期期中化学试卷(解析版) 题型:选择题
我国的“神州六号”载人飞船已发射成功,“嫦娥”探月工程已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的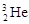 ,每百吨
,每百吨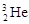 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以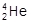 的形式存在。下列说法正确的是( )
的形式存在。下列说法正确的是( )
A. 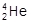 原子核内含有4个质子
原子核内含有4个质子
B. 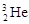 和
和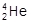 互为同位素
互为同位素
C. 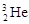 原子核内含有3个中子
原子核内含有3个中子
D. 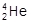 最外层电子数为2,所以
最外层电子数为2,所以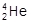 具有较强的金属性
具有较强的金属性
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高一下学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.还原性:K> Na > Mg
B.氢化物的稳定性:H2O < H2S < H2Se
C.酸性:H3PO4< H2SO4< HCl
D.原子半径:Na< Mg < Al
查看答案和解析>>
科目: 来源:2015-2016学年新疆农业大学附中高一下学期期中化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的位置如图,其中M为地壳中含量最高的金属元素。下列说法不正确的是 ( )
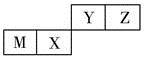
A. 原子半径Z<M
B. Y的最高价氧化物对应水化物的酸性比X的弱
C. X的最简单气态氢化物的热稳定性比Z的弱
D. Z位于元素周期表中第2周期、第ⅥA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com