
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法中有明显错误的是( )
A.对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大
B.升高温度,一般可使活化分子的百分数增大,分子间的碰撞频率提高,因而反应速率增大
C.活化分子之间发生的碰撞不一定为有效碰撞
D.加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大反应速率
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
一定条件下,在2L的密闭容器中充入2molSO2和一定量的O2,发生反应2SO2(g)+O2(g)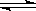 2SO3(g),进行到4min时,测得n(SO2)=0.4mol,若反应进行到前2min末时,容器中n(SO2)为( )
2SO3(g),进行到4min时,测得n(SO2)=0.4mol,若反应进行到前2min末时,容器中n(SO2)为( )
A.1.6mol B.1.2mol C.大于1.6mol D.小于1.2mol
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
已知反应A2(g)+2B2(g)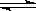 2AB2(g),△H<0,下列说法正确的是( )
2AB2(g),△H<0,下列说法正确的是( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,减小压强或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)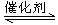 2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
下列热化学方程式中△H代表燃烧热的是( )
A.CH4(g)+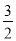 O2(g)=2H2O(l)+CO(g)△H1
O2(g)=2H2O(l)+CO(g)△H1
B.S(s)+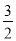 O2(g)=SO3(s)△H2
O2(g)=SO3(s)△H2
C.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H3
D.2CO(g)+O2(g)=2CO2(g)△H4
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)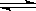 NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g)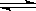 H2(g)+I2(g).达到平衡时,c(H2)=0.5mol/L,c(HI)=3mol/L,则此温度下反应①的平衡常数为( )
H2(g)+I2(g).达到平衡时,c(H2)=0.5mol/L,c(HI)=3mol/L,则此温度下反应①的平衡常数为( )
A.9 B.16 C.12 D.25
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)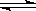 2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是( )
2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是( )
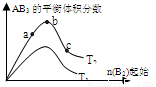
A.正反应一定是放热反应
B.若T2>T1,则正反应一定是吸热反应
C.达到平衡时A2的转化率大小为:b>a>c
D.b点时,平衡体系中A、B原子数之比接近3:1
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)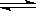 2NH3(g)+Q,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示.下列叙述正确的是( )
2NH3(g)+Q,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示.下列叙述正确的是( )
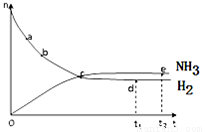
A.点a的正反应速率比点b的小
B.点 c处反应达到平衡
C.点d(t1时刻) 和点 e(t2时刻) 处n(N2)不一样
D.点d(t1时刻) 和点 e(t2时刻) 处H2的转化率相同
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)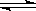 Ni(CO)4(g),已知该反应平衡常数与温度的关系下表:下列说法正确的是( )
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表:下列说法正确的是( )
温度℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
D.25℃时反应Ni(CO)4(g)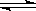 Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州中学高二上第一次月考化学试卷(解析版) 题型:选择题
对于反应N2O4(g)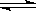 2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上任何一点为对应压强下的平衡点),下列说法正确的是( )
2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上任何一点为对应压强下的平衡点),下列说法正确的是( )
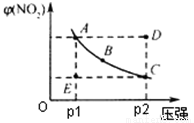
A.A、C两点的正反应速率的关系为A>C
B.A、B、C、D、E各状态中,v(正)<v(逆)的是状态E
C.维持p1不变,E→A所需时间为x;维持p2不变,D→C所需时间为y;则x<y
D.使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是从p1突然加压到p2,再由p2无限缓慢降压至p1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com