
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:选择题
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌?锰碱性电池以氢氧化钾溶液为电解液,电池反应式为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池工作时,电子由正极通过外电路流向负极
C.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-===Mn2O3(s)+2OH-(aq)
D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:选择题
对可逆反应2A(s)+3B(g)?C(g)+2D(g) △H<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高.
A.①② B. ③ C. ④ D.④⑤
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W、R的原子序数依次增大,其中前四种元素原子的最外层电子数之和为14。X是周期表中原子半径最小的元素,Z是短周期中金属性最强的元素,Y与W同主族。下列说法不正确的是( )
A. 原子半径:X<W<Z
B. 最高价氧化物对应水化物的酸性:W>R
C. R在周期表中的位置为第三周期ⅦA族
D. 简单气态氢化物的热稳定性:Y>W
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:选择题
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol/L。下列判断正确的是( )
xC(g)+2D(s)。2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.4mol/L。下列判断正确的是( )
A.x =1
B.A的平均反应速率为0.3mol/(L·s)
C.B的转化率为60%
D.若混合气体的密度不再改变时,该反应一定达到平衡状态
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:填空题
A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C位于第___周期____族,它的最高价氧化物的化学式为___________。
(2)A与D形成稳定化合物的化学式为______________,该化合物的晶体类型是________。写出该化合物与CO2反应的化学方程式 。
(3 )C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为______________。
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:填空题
在容积为2L的密闭容器中进行如下反应:
A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
(1)5min末A的物质的量浓度为__________ mol/L·
(2)前5min内用B表示的化学反应速率v(B)为___________ mol/(L·min)。
(3)化学方程式中n值为__________。
(4)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol/(L·min)
②v(B)=6mol/(L·min)
③v(C)=4.5mol/(L·min)
④v(D)=8mol/(L·min)
其中反应速率最快的是__________(填编号)。
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:填空题
(1)研究NO2、SO2、CO等大气污染气体的处理具有重要意义。 已知:
2SO2(g)+O2(g) 2SO3(g) ΔH= -196.6kJ·mol-1
2NO(g)+O2(g)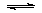 2NO2(g) ΔH= -113.0kJ·mol-1
2NO2(g) ΔH= -113.0kJ·mol-1
则反应NO2(g)+SO2(g)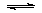 SO3(g)+NO(g)的ΔH= kJ·mol-1
SO3(g)+NO(g)的ΔH= kJ·mol-1
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:
N2(g)+3H2(g)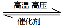 2NH3(g)。
2NH3(g)。
在一定条件下,将一定量的N2和H2的混合气体充入某定容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是 (填序号)。
A.容器中混合气体的密度不随时间变化
B.断裂3 mol H-H键的同时形成6 mol N-H键
C.N2 、H2 、NH3的物质的量之比为1:3:2
D.容器中的压强不随时间变化
(3)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则该反应的热化学方程式是____________。
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:填空题
由A、B、C、D四种金属按下表中装置图进行实验.
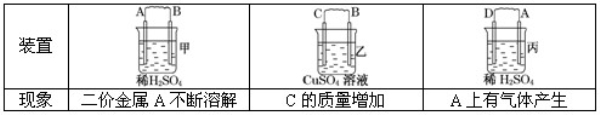
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_____________________________________.
(2)装置乙中正极的电极反应式是____________________________________..
(3)四种金属活泼性由强到弱的顺序是__________________________________.
(4)A、C形成合金,露置在潮湿空气中,_______先被腐蚀。
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:填空题
从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量 用来衡量一个国家的石油化工发展水平.B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与 氢元素的质量比为12:1,B的相对分子质量为78.回答下列问题:
(1)A的电子式 B的结构简式
(2)A使溴的四氯化碳溶液褪色的化学反应方程式: ,反应类型: ;
(3)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式: ,
反应类型: 。
查看答案和解析>>
科目: 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:实验题
实验室制乙酸乙酯得主要装置如图中A所示,主要步骤:
①在a试管中按2∶3∶2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2 mL产物时停止加热。撤下b试管并用力振荡,然后静置待其中液体分层;
⑤分离出纯净的乙酸乙酯。
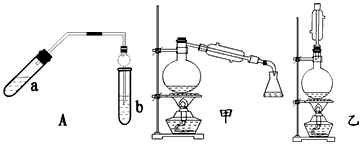
请回答下列问题:
(1)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:________
(2)A装置中使用球形管除起到冷凝作用外,另一重要作用是_____________________;步骤⑤中分离乙酸乙酯必须使用的一种仪器是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com