
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:简答题
经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.
(1)pM2.5的雾霾中能形成酸雨的物质是_______.
(2)为消除NOx对环境的污染,可利用NH3在一定条件下与NO反应生成无污染的气体.
已知: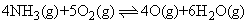 △H=-900.0 kJ·moL-1
△H=-900.0 kJ·moL-1
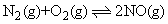 △H=+180.0 kJ·moL-1
△H=+180.0 kJ·moL-1
已知NH3(g)与NO(g)在一定条件下反应,生成无污染气体,请写出转化过程的热化学反应方程式___________________.
(3)对于反应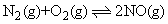 ,在恒温恒容条件下,向密闭容器中加入等物质的N2和O2.下列方法中可以说明可逆反应已达平衡状态的是____________.
,在恒温恒容条件下,向密闭容器中加入等物质的N2和O2.下列方法中可以说明可逆反应已达平衡状态的是____________.
a.容器内压强不再变化
b.混合气体密度不再变化
c.混合气体的平均相对分子质量不再变化
d.NO的质量分数不再变化
(4)下图电解装置可将雾霾中的SO2、NO转化为(NH4)2SO4,阴极的电极反应式是________,物质A是_________(填名称)

查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:简答题
常温下,将某一元酸HA溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
(1)在①组实验中0.1 mol·L-1HA溶液中水的电离程度为a,0.1 mol·L-1NaOH溶液中水的电离程度为b,所得混合溶液中水的电离程度为c.则a、b、c由大到小的顺序是_________.
(2)在②组实验中c_____0.2(填“<”、“>”或“=”)
(3)根据③组实验所得的混合溶液,其溶液中离子浓度大小排列顺序是____________.
(4)常温下,已知KSP[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于_________.
查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:实验题
硫酸锰铵[(NH4)2SO4·MnSO4·nH2O]是浅粉色晶体,易溶于水,在农业上用作微量元素肥料.实验室由MnO2制备硫酸锰铵的实验步骤如下:
①在烧杯中加入20.0 ml,1 mol·L-1硫酸并加入a g草酸微热,再慢慢分次加入a g MnO2,盖上表面皿,使其充分反应.
②煮沸溶液并趁热过滤.
③往热滤液中加入b g硫酸铵,待硫酸铵全部溶解后,在冰水浴中冷却,30分钟后过滤,并用少量乙醇溶液洗涤两次,用滤纸吸干或放在表面皿上干燥.
④称得产品质量为c g.
根据以上信息,回答下列问题:
(1)配制100 mL 1 mol·L-1硫酸溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外,还需要__________.
(2)MnO2与草酸的硫酸溶液反应的化学方程式为____________.
(3)用乙醇洗涤的目的是___________________.
(4)为确定其化学式,现对产品在氮气中进行热重分析,已知在371℃下结晶水会全部失去.其TG曲线如图所示.
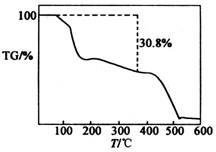
(TG=固体样品的剩余质量/固体样品的起始质量×100%)
则(NH4)2SO4·MnSO4·nH2O中的n=______(填数字,取整数)
查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:推断题
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A原子的半径最小,B原子的价电子排布式为nsnnpn,D是地壳中含量最多的元素,E元素原子序数为26.
(1)D2-的结构示意图为___________.
(2)运用等电子体理论可知,1 mol BD中含有π键的数目为___________NA.
(3)BD32-中心原子杂化轨道的类型为___________杂化;A4C2D3所含的化学键有__________________.
(4)E元素的基态原子价电子排布式为___________.
(5)以上五种元素最高价氧化物对应水化物的酸性最强的酸是___________ (用分子式表示)
(6)用电子式表示A2D的形成过程_________________________________.
查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:推断题
现有A、B、C、D、E五种元素,原子序数依次增大,且不超过36.A元素的基态原子最外层电子数是次外层的三倍;B元素的基态原子核外有13种不同运动状态的电子;C与B同一周期,原子中未成对电子数是同周期中最多的;D2-的核外电子排布与氩原子相同;E元素的基态原子价电子排布式为3d104s1.请根据相关信息,回答下列问题:
(1)在A、B、C、D四种元素中第一电离能最小的是___________,电负性最大的是___________ (用相应的元素符号表示)
(2)写出DA2的水化物在水中的电离方程式___________.DA3是___________分子(填“极性”或“非极性”)
(3)A、C的简单氢化物中,哪种物质的沸点高,原因是什么? ___________________________
(4)若[E(NH3)4]2+具有对称的空间构型,且当[E(NH3)4]2+中的两个NH3分子被两个Cl-取代时,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为_________ (填序号)
a.正四面体 b.平面正方形 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为a pm,密度为dg·cm-3(1pm=10-10cm)写出阿伏加德罗常数NA的表达式___________.(用M、a、d表示)
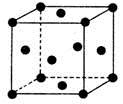
查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:实验题
—硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)
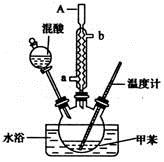
实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸);
②在三颈烧瓶里装15 mL甲苯(密度为0.866 g·cm-3);
③装好其他药品,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,大约反应10分钟至三颈烧瓶底有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯共15 g.
根据上述实验,回答下列问题:
(1)本实验的关键是控制温度在30℃左右,如果温度过高,则会产生__________等副产品(填物质名称)
(2)简述配制混酸的方法:____________________.
(3)A仪器名称是__________,进水口是__________.
(4)写出甲苯与混酸反应生成对硝基甲苯的化学方程式:___________________________.
(5)分离产品方案如下:
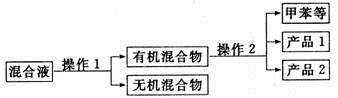
操作2的名称是___________.经测定,产品2的核磁共振氢谱中有5个峰,它的名称为___________.
(6)本实验中一硝基甲苯的产率为___________ (结果保留三位有效数字)
查看答案和解析>>
科目: 来源:2015-2016学年湖北省黄冈市高二下期末化学试卷(解析版) 题型:推断题
某有机物E的合成路线如下:
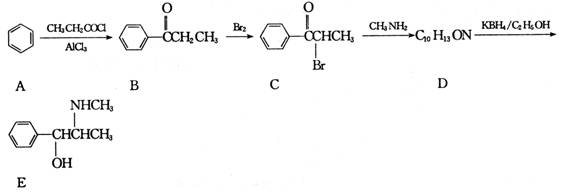
回答下列问题:
(1)B的分子式为___________;C中含有的官能团有___________ (写名称)
(2)写出C→D反应的化学方程式:___________.A→B的反应类型为___________.
(3)C的消去产物可以合成高分子化合物F,请写出F的结构简式:___________.
(4)能发生银镜反应B的同分异构体有_________种.
(5)已知: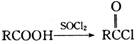
参照上述合成路线,设计一条由苯和乙酸为起始原料制备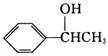 的合成路线:__________________________________________________________________.
的合成路线:__________________________________________________________________.
查看答案和解析>>
科目: 来源:2015-2016学年云南省高一下学期期末化学试卷(解析版) 题型:选择题
下列做法中,不利于让德宏实现 “天更蓝,水更清”目标的是( )
A.推广使用无磷洗涤剂
B.推广使用脱硫煤
C.减少汽车尾气排放
D.任意排放污水
查看答案和解析>>
科目: 来源:2015-2016学年云南省高一下学期期末化学试卷(解析版) 题型:选择题
下列化学用语书写正确的是( )
A.氨的电子式: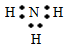
B.烯烃中所含官能团的结构简式:C = C
C.铜、锌与稀硫酸组成的原电池的负极反应:Zn - 2e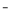 =
=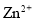
D.铝热法炼铁的化学方程式:Fe + Al2O3 Al + Fe2O3
Al + Fe2O3
查看答案和解析>>
科目: 来源:2015-2016学年云南省高一下学期期末化学试卷(解析版) 题型:选择题
某些建筑材料含有放射性元素氡( ),会对人体产生一定危害。研究表明氡的α射线会致癌,WHO认定的19种致癌因素中,氡为其中之一,仅次于吸烟。该原子中中子数和质子数之差是( )
),会对人体产生一定危害。研究表明氡的α射线会致癌,WHO认定的19种致癌因素中,氡为其中之一,仅次于吸烟。该原子中中子数和质子数之差是( )
A. 136 B. 50 C. 86 D. 222
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com