
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A.通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极区反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O===2Zn(OH) 。下列说法正确的是
。下列说法正确的是
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中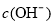 逐渐减小
逐渐减小
C.放电时,负极反应为:Zn+4OH–?2e–===Zn(OH)
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
有关下列四个常用电化学装置的叙述中,正确的是
|
|
|
|
图Ⅰ 碱性锌锰电池 | 图Ⅱ 铅-硫酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
A.图Ⅰ所示电池中,MnO2的作用是催化剂
B.图II所示电池放电过程中,硫酸浓度不断增大
C.图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图IV所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
加热条件下,将24.0gCuO和Fe2O3的混合物与足量的CO完全反应,并将反应后的气体全部通入到足量的澄清石灰水中,得到白色沉淀40.0g。下列有关叙述中不正确的是

A.原混合物中CuO和Fe2O3的物质的量的比为1:1
B.参加反应的CO的质量为11.2g
C.原混合物中Fe元素的质量为5.6g
D.原混合物中CuO的质量分数约为33.3%
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
臭氧(O3)的制备方法很多,其中电解水法的原理如下图所示,
下列有关说法不正确的是
A.可向水中加入NaCl提高水的导电性
B.b电极周围pH减小
C.a电极的电极反应式为
D.a电极为阴极,b电极为阳极
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
已知ClO2常温下呈气态,其分子构型与水分子相似,在自然环境中ClO2最终变为Cl-。下列说法正确的是
A.ClO2的分子结构呈V型,属非极性分子
B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子数目表示)是Cl2的5倍
C.ClO2、Cl2的稀溶液用于环境消毒,对人体无任何危害
D.常用Na2SO3在H2SO4存在条件下,还原NaClO3来制ClO2,化学方程式为:Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:选择题
将7.28g Fe溶于过量的稀H2SO4中,在加热的条件下,用2.02gKNO3去氧化溶液中Fe2+,待反应完全后,剩余Fe2+还需0.4mol/L KMnO4溶液25mL才能完全氧化,则KNO3的还原产物
A.NO B.NO2 C.N2O D.N2O3
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:填空题
(1)用零价铁(Fe)去除水体中的硝酸盐(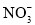 )已成为环境修复研究的热点之一。Fe还原水体中
)已成为环境修复研究的热点之一。Fe还原水体中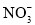 的反应原理如右图所示。
的反应原理如右图所示。
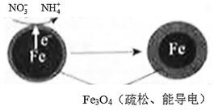
①作负极的物质是________。②正极的电极反应式是________ _。
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)  CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)  CO(g) +H2O(g) △H3
CO(g) +H2O(g) △H3
已知反应①中相关的化学键键能数据如下:
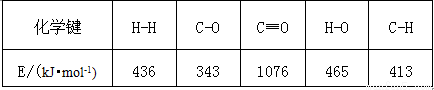
由此计算△H1= kJ·mol-1.已知△H2= –58kJ·mol-1,则△H3= kJ·mol-1.
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:实验题
NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(解析版) 题型:填空题
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)R基态原子的电子排布式是 ,X和Y中电负性较大的是 (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是___________。
(3)X与M形成的XM3分子的空间构型是__________。
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是_________(填离子符号)。
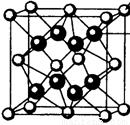
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com