
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
下列各项中表达正确的是
A.第VⅡA族元素形成的氢化物中沸点最高的是HI
B.第三周期元素形成的简单离子中,半径最小的是Al3+
C.用电子式表示HCl形成过程: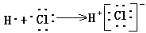
D.水分子很稳定性是因为水分子间易形成氢键
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
已知一定温度和压强下,合成氨反应:N2(g)+3H2(g)  2NH3(g);△H=-92.0KJ·mol-1将1mol N2和3mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时在该容器中充入2mol NH3,s反应达到平衡时的热量变化是
2NH3(g);△H=-92.0KJ·mol-1将1mol N2和3mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时在该容器中充入2mol NH3,s反应达到平衡时的热量变化是
A.吸收18.4KJ热量
B.放出18.4KJ热量
C.吸收73.6KJ热量
D.放出73.6KJ热量
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
热激活电池可用作火箭.导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca =CaCl2+Li2SO4+Pb。
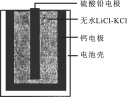
下列有关说法正确的是
A .正极反应式:Ca+2Cl- - 2e- =CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针不偏转
D.每转移0.1mol电子,理论上生成20.7g Pb
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
下列有关热化学方程式书写及对应表述均正确的是( )
A.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6kJ.mol-1
B.稀醋酸与0.1mol/L NaOH溶液反应:H +(aq)+OH -(aq)═H2O(l) △H= -57.3kJ/mol
C.已知1mol氢气完全燃烧生成液态水所放出的热量为285.5kJ,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5kJ.mol-1
D.已知2C(s)+O2(g)═2CO(g)△H=-22.1kJ.mol-1则可知C的燃烧热△H=-110.5kJ.mol-1
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
(1)将1.0 mol CH4和2.0molH2O(g)通入容积固定为10 L的反应容器中,在一定条件下发生反应:CH4(g)+H2O(g)  CO (g)+3H2(g) ,测得在一定的压强下CH4的转化率与温度的关系如图1。
CO (g)+3H2(g) ,测得在一定的压强下CH4的转化率与温度的关系如图1。
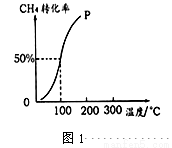
①该反应的ΔH 0(填“>”“<”或“=”)
②假设100 ℃时达到平衡所需的时间为3 min,则用H2表示该反应的平均反应速率为 mol/(L·min)。
③100℃时该反应的平衡常数的数值为 。
④可用来判断该反应达到平衡状态的标志有 (填字母)。
A.CO的含量保持不变
B.CH4浓度与CO浓度相等
C.ν正(CH4)=3ν逆(H2)
D.混合气体的密度保持不变
E.混合气体的总物质的量保持不变
F.混合气体的压强度保持不变
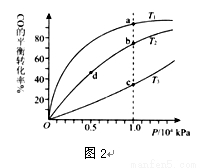
(2)生成甲醇的反应:CO(g)+2H2(g) CH3OH(g) △H =—129.0 kJ/mol,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示。下列说法正确的是 (填字母)。
CH3OH(g) △H =—129.0 kJ/mol,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示。下列说法正确的是 (填字母)。
A.温度:T1>T2 > T3
B.正反应速率:ν(a)>ν(c); ν(b)>ν(d)
C.平衡常数: K(a)>K(c) ; K(b)=K(d)
D.平均摩尔质量:M(a) >M(c); M(b)>M(d)
(3)工业上利用甲醇制备氢气的常用方法之一为:甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)  CO(g)+2H2(g),此反应能自发进行的原因是 。
CO(g)+2H2(g),此反应能自发进行的原因是 。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H2O(l)=H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+2O2(g)=2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)= N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式___________。
(5)已知: ①N2 (g) + 2O2 (g) = 2NO2 (g) △H = + 67.7kJ/mol
②N2H4 (g) +O2 (g) = N2(g) +2H2O (g) △H = -543kJ/mol
③1/2H2 (g) + 1/2F2 (g) = HF (g) △H = -269kJ/mol
④H2 (g) + 1/2O2 (g) = H2O (g) △H = -242kJ/mol
有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的热化学方程式: 。
(6)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) == 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) ==C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) == 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2 (g) == 2H2O(l) ΔH=-d kJ·mol-1 (abcd均为正值)
请回答下列问题:
判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 ______(填“大于”、“等于”或“小于”)途径II放出的热量。由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量。
b 与a、c、d的数学关系式是______________。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
利用天然气热裂解制取乙炔和氢气近年来成为各国研究的热点,发生的主要反应为:2CH4(g) C2H2(g)+3H2(g) △H=a kJ•mol-1,副反应:2CH4(g)
C2H2(g)+3H2(g) △H=a kJ•mol-1,副反应:2CH4(g) C2H4(g)+2H2(g) 回答下列问题:
C2H4(g)+2H2(g) 回答下列问题:
(1)天然气热裂解过程使用的催化剂中含有SiO2、Al2O3等多种难被还原的氧化物,写出SiO2的另外两种用途:_______________________,写出Al2O3与苛性钾溶液反应的离子方程式___________________;
(2)已知甲烷的燃烧热△H=-890.3kJ•mol-1,乙炔的燃烧热△H=-1299.6kJ•mol-1,氢气的燃烧热△H=-285.8kJ•mol-1,则上式中的a=___________;
(3)天然气经重整催化作用生成氢气,氢气在下图所示的燃料电池中放电(以熔融Li2CO3和K2CO3为电解质),写出燃料极上发生的电极反应式_______________________________;

(4)某温度下,向1L恒容密闭容器中充入0.3mol甲烷,控制条件使其只发生上述副反应,达到平衡时,测得c(C2H4)=c(CH4),则该条件下甲烷的平衡转化率为__________;
(5)天然气裂解过程中,平衡时各气体分压(单位为Pa)的对数(δ)与温度(T)之间的关系如下图:

①副反应2CH4(g) C2H4(g)+2H2(g) 的△H__________(填“>”或“<”)0;
C2H4(g)+2H2(g) 的△H__________(填“>”或“<”)0;
②利用图中数据计算A点温度下主要反应2CH4(g) C2H2(g)+3H2(g)的平衡常数__________(利用平衡分压代替平衡浓度计算,
C2H2(g)+3H2(g)的平衡常数__________(利用平衡分压代替平衡浓度计算, )。
)。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
A、B、C、D、E五种元素的原子序数依次增大,且均小于18;A原子的最外层比B原子的最外层少2个电子,A原子的最外层电子数是次外层电子数的两倍;A、B、C三种元素能结合成化合物C2AB3,在1 mol C2AB3中共有52 mol电子;0.5mo1D元素的单质与酸全部反应时,有9.03×1023个电子转移,在B与D形成的化合物中,D的质量分数为52.94%,D原子核内有14个中子;每个E原子与氢原子化合时只生成了一个共价键。试填写下列空白:
(1)元素的名称D ,E 。
(2)C在B中燃烧生成的化合物的化学式
(3)A.B.C结合成的化合物的化学式是 。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:填空题
已知:将KI.盐酸.试剂X和淀粉四种溶液混合,无反应发生。若再加入双氧水,将发生反应:H2O2+2H++2I—→2H2O+I2,且生成的I2立即与试剂X反应而被消耗。一段时间后,试剂X将被反应生成的I2完全消耗。由于溶液中的I—继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝。因此,根据试剂X的量.滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I—→2H2O+I2的反应速率。
下表为某同学依据上述原理设计的实验及实验记录(各实验均在室温条件下进行):
编 号 | 往烧杯中加入的试剂及其用量(mL) | 催化剂 | 溶液开始变蓝时间(min) | ||||
| H2O |
X 溶液 |
|
| |||
1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 无 | 1.4 |
2 | 20.0 | m | 10.0 | 10.0 | n | 无 | 2.8 |
3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 无 | 2.8 |
4 | 20.0 | 0 | 10.0 | 10.0 | 40.0 | 无 | t |
5 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
回答下列问题:
(1)已知:实验1、2的目的是探究H2O2浓度对H2O2+2H++2I—→2H2O+I2反应速率的影响。实验2中m= ,n=
(2)一定温度下,H2O2+2H++2I—→2H2O+I2反应速率可以表示为v=k·c a(H2O2)·c b (I—)·c(H+)(k为常数),则:
①实验4时,烧杯中溶液开始变蓝的时间t=___________。
②根据上表数据可知,a、b的值依次为 和 。
(3)实验5表明:硫酸铁能提高反应速率。
①催化剂能加快反应速率是因为催化剂 (填“提高”或“降低”)了反应活化能。
②试用离子方程式表示Fe2(SO4)3对H2O2+2H++2I—→2H2O+I2催化的过程。
. (不必配平)
查看答案和解析>>
科目: 来源:2015-2016学年湖北省、黄陂一中高二下期末化学试卷(解析版) 题型:选择题
化学在绿色发展、循环发展、低碳发展及推进生态文明建设中正发挥着积极作用,下列做法不正确的是( )
A.研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.铁强化酱油可通过膳食补充人体所需的铁元素
D.地沟油由于混有一些对人体有害的杂质而不能食用,可加工制成生物柴油,生物柴油成分与从石油中提取的柴油成分不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com