
科目: 来源:2015-2016学年新疆伊犁州伊宁二中高二下期末化学试卷(解析版) 题型:填空题
A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”)。
(2)当n=3时, A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是
(用元素符号表示)。
(4)C是 ,最高价氧化物的水化物是 (用元素符号表示)。
(5)已知某红紫色配合物的组成为[Co(NH3)5(H2O)]Cl3。该配合物中的中心离子钴离子在基态时核外电子排布式为 ,中心离子钴离子的配位数是 ,
查看答案和解析>>
科目: 来源:2015-2016学年新疆伊犁州伊宁二中高二下期末化学试卷(解析版) 题型:填空题
下表列出了前20号元素中的某些元素性质的一些数据:
元素 | A | B | C | D | E | F | G | H | I | J |
原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
最高 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
最低 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)以上10种元素中,电负性最大的是________(填元素符号)。
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物反应:_________ _____。
②B2C2与EC2反应:____________ ____。
(3)A元素原子核外电子排布图是__ ___;比元素B原子序数大11的元素的原子的电子排布式是 ______。
(4)C和I相比较,非金属性较弱的是_____(填元素名称)。
查看答案和解析>>
科目: 来源:2015-2016学年新疆伊犁州伊宁二中高二下期末化学试卷(解析版) 题型:填空题
(12分) 东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_ _,提供孤电子对的成键原子是__ ___。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是____ ;氨是____ _分子(填“极性”或“非极性”),中心原子的轨道杂化类型为____。
(3)单质铜及镍都是由______键形成的晶体:元素同与镍的第二电离能分别为:I(Cu)=1959kJ/mol,I(Ni)=1753kJ/mol,I(Cu)>I(Ni)的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
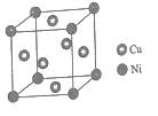
晶胞中铜原子与镍原子的数量比为_____。
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
原子结构模型的简历和发展与科学实验紧密相关.下列对应关系错误的是
A. 道尔顿发现原子——“空心球”模型
B. 汤姆逊发现电子——“葡萄干布丁”模型(原子中负电荷电子均匀排布)
C. 卢瑟福进行α粒子散射实验——“核式”模型(正电荷集中在原子核)
D. 玻尔解释氢原子光谱——“电子分层排布”模型
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
下列化学用语的书写正确的是
A.羟基的电子式: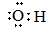
B.过氧化氢的电子式:
C.As的原子的特征电子排布式:[Ar]4s14p3
D.基态Mg原子的核外电子排布图:
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 电子云通常是用小黑点来表示电子的多少
B. 在同一能级上运动的电子,其运动状态是相同的
C. 能层序数越大,s电子云的半径越大
D. 电子仅在激发态跃迁到基态时才会产生原子光谱
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
下列不能根据元素电负性判断元素
A. 是金属还是非金属
B. 正负化合价
C. 化学键类型
D. 化合物溶解度
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
下列有关物质性质的比较,不正确的是
A. 金属性:Li>Na>K>Rb
B. 酸性:HF<HCl<HBr<HI
C. 微粒半径:K+>Na+>Mg2+>Al3+
D. 酸性:HClO4>H2SO4>H3PO4>H2SiO3
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
在通常条件下,下列各组物质的性质排列正确的是
A. Na、Mg、Al的第一电离能逐渐增大
B. 热稳定性:HF>H2O>NH3
C. S2﹣、Cl﹣、K+的半径逐渐增大
D. O、F、Ne的电负性逐渐增大
查看答案和解析>>
科目: 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
五种短周期元素的某些性质如下表所示,其中W、Y、Z为同周期元素,下列说法正确的是
元素代号 | X | W | Y | Z | Q |
原子半径(×10-12m) | 37 | 64 | 66 | 70 | 154 |
主要化合价 | +1 | -1 | -2 | +5、-3 | +1 |
A.Z与X之间形成的化合物具有还原性
B.由Q与Y形成的化合物中只存在离子键
C.由X、Y、Z三种元素形成的化合物的水溶液呈碱性
D.Y与W形成的化合物中,Y显负价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com