
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液。下列有关叙述正确的是
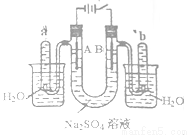
A.逸出气体的体积,A电极的小于B电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.A电极附近呈红色,B电极附近呈蓝色
D.电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶解呈中性
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
在相同温度和压强下,对反应CO2(g)+H2O(g) CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内的各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内的各组分的物质的量见下表
物质 物质的量 实验 | CO2 | H2 | CO | H2O |
甲 | a mol | a mol | 0mol | 0mol |
乙 | 2a mol | a mol | 0mol | 0mol |
丙 | 0mol | 0mol | a mol | a mol |
丁 | a mol | 0mol | a mol | a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B.乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
已知在酸性溶液中,下列物质氧化H2S生成S是时,自身发生如下变化: IO3-→I2; Fe3+→Fe2 +; SO2→S;MnO4-→Mn2+ 。如果分别用等物质的量的这些物质氧化足量的H2S,得到S最多的是( )
A.IO3- B.Fe3+ C.SO2 D. MnO4-
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
分子式为C5H8O3的有机物能使新制Cu(OH)2悬浊液溶解,加热后出现砖红色沉淀,则该有机物的结构有(不含立体异构)
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
电渗析法是一种利用离子交换膜进行海水淡化的方法,工作原理如图。下列有关说法错误的是
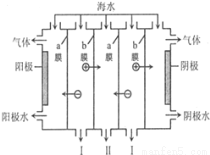
A.阳极可发生电极反应:2Cl--2e-═Cl2↑
B.阴极附近溶液的pH减小
C.a膜为阴离子交换膜,b膜为阳离子交换膜
D.I、II分别是淡水、浓海水出口
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
固体碘化铵置于密闭容器中,加热至一定温度后恒温,容器中发生反应:①NH4I(s) NH3(g)+HI(g) ②2HI(g)
NH3(g)+HI(g) ②2HI(g) H2(g)+I2(g),测得平衡时c(I2)=0.5mol/L,反应①的平衡常数为20mol2/L2,则下列结论不正确的是
H2(g)+I2(g),测得平衡时c(I2)=0.5mol/L,反应①的平衡常数为20mol2/L2,则下列结论不正确的是
A.平衡时c(NH3)=5mol/L
B.平衡时HI分解率为20%
C.混合气体的平均摩尔质量不再发生变化不可以作为判断该反应达到平衡状态的标志
D.平衡后缩小容器体积,NH4I的物质的量增加,I2的物质的量不变
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
COCl2的分解反应为COCl2(g) Cl2(g)+CO(g)。将一定量COCl2(g)和Cl2(g)放入一密闭容器中,2min时达到平衡后,各物质的物质的量在不同条件下的变化情况如下图所示。
Cl2(g)+CO(g)。将一定量COCl2(g)和Cl2(g)放入一密闭容器中,2min时达到平衡后,各物质的物质的量在不同条件下的变化情况如下图所示。
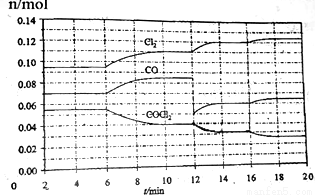
下列相关说法中不正确的是
A.1min时以CO表示的逆反应速率小于3min时以CO表示的正反应速率
B.若在6min时改变的条件为升高温度,则反应的平衡常数K增大
C.12min时改变的条件可为减小CO的浓度,16min时改变的条件可为增大反应容器的体积
D.以CO表示在4~5min、10~11min和12~13min时平均反应速率为v(4~5)<v(10~11)<v(12~13)
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:填空题
用铅蓄电池连接惰性电极电解一定量的CuSO4溶液,请回答下列问题:
(1)铅蓄电池放电时正极的电极反应式为________________________________;
(2)惰性电极电解CuSO4溶液的离子方程为_____________________;
(3)若电解一段时间后向电解池溶液中加入1molCu(OH)2·CuCO3,可以使该溶液恢复至原来的浓度和体积,则在该电解过程中转移电子的数目为___________,该电解过程中铅蓄电池中消耗的H2SO4和电解池中生成的H2SO4的物质的量之比为____________。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:填空题
与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,请回答下列问题:
(1)该电池放电时生成+3价铁的化合物,则电池放电时正极的电极反应式为____________________;
(2)完成制备电池正极材料过程中某一反应的化学方程式:
________FeCl3+________NaOH+________NaClO=________Na2FeO4+________+________
(3)FeO42-具有强氧化性,在其钾盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式为____________________。
查看答案和解析>>
科目: 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:填空题
下表为长式周期表的一部分,其中的编号代表对应的元素。
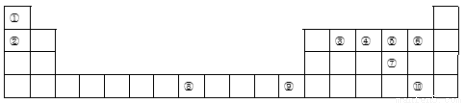
(1)比较①和②具有相同核外电子排布的简单离子半径大小关系为______________(填化学式);③、④、⑤三种元素的第一电离能由大到小的顺序为____________(填元素符号),写出原子序数和元素⑧相差2且元素⑧同族的元素基态原子的外围电子排布式____________。
(2)在元素③与①形成的原子个数比为1:1的四原子分子中,③原子的杂化方式为____________。其分子中δ键和π键数目之比为____________。
(3)元素④的某种氢化物甲分子中含有18个电子,甲为二元弱碱,在水中的电离方程式与氨相似。写出甲在水中的第一步电离的电离方程式____________。甲在微电子工业中,可作刻蚀剂H2O2的清除剂,二者发生反应的产物不污染环境,其化学方程式为____________。
(4)元素⑥和⑤形成分子乙的结构与元素①和⑤形成的最简单分子丙相似,乙的VSEPR模型为___________,解释丙的沸点高于乙的原因____________。
(5)可用赤血盐K3[Fe(CN)6]检验元素⑧的+2价阳离子,写出该反应的离子方程式___________,元素⑩的阴离子与元素⑧的+2价离子形成化合物丁,将3molCl2通入含4mol丁的溶液,用一个离子方程式表示该反应过程为____________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为⑦和⑨组成的离子化合物戊的晶胞,其中三个离子(白色球)坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D离子(黑色球)的坐标参数为_____。
,0)。则D离子(黑色球)的坐标参数为_____。
②晶胞参数,描述晶胞的大小和形状,已知戊的晶胞参数apm,则晶胞中B和D离子的距离为______pm。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com