
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:选择题
对于平衡体系:mA(g)+ nB(g) pC(g)+ qD(g),下列判断正确的是( )
pC(g)+ qD(g),下列判断正确的是( )
A.若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.45 倍,则m+n>p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
C.若升高平衡体系的温度,达到新平衡时A 的浓度变为原来的0.55 倍,说明该反应△ H<0
D.若平衡后同时增大A、B的浓度,则A、B的转化率一定都减小
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:选择题
已知图一表示的是可逆反应CO(g)+H2(g) C(s)+H20(g) △H >0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H20(g) △H >0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g) N2O4(g) △H<0 的浓度(c)随时间t的变化情况。下列说法中正确的是( )
N2O4(g) △H<0 的浓度(c)随时间t的变化情况。下列说法中正确的是( )
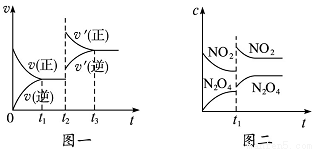
A.图一t2时改变的条件可能是升高了温度或增大了压强
B.若图一t2时改变的条件是增大压强,则反应的△H增大
C.图二t1时改变的条件可能是升高了温度或增大了压强
D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:选择题
下列四种情况不能用下图图像表示的是( )

A.N2(g)+3H2(g) 2NH3(g),恒容充入He,N2的转化率与时间的关系
2NH3(g),恒容充入He,N2的转化率与时间的关系
B.CH4(g)+H2O(g) CO(g)+3H2(g);ΔH>0,平衡后CH4的物质的量与△H的关系
CO(g)+3H2(g);ΔH>0,平衡后CH4的物质的量与△H的关系
C.FeCl3+3KSCN Fe(SCN)3+3KCl,平衡后加入KCl固体,c(Cl—)与正反应速率关系
Fe(SCN)3+3KCl,平衡后加入KCl固体,c(Cl—)与正反应速率关系
D.H2(g)+I2(g) 2HI(g),平衡后缩小容器容积,速率与时间的关系
2HI(g),平衡后缩小容器容积,速率与时间的关系
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:选择题
已知某化学反应的平衡常数表达式为K=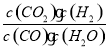 ,在不同的温度下该反应的平衡常数值分别为:
,在不同的温度下该反应的平衡常数值分别为:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述不正确的是
A.该反应的化学方程式是:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO2和H2各1mol,5min后温度升高到830℃,此时测得C为0.4mol时,该反应为平衡状态
D.某温度下,如果平衡浓度符合下列关系式: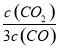 =
=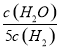 ,判断此时的温度是1000 ℃
,判断此时的温度是1000 ℃
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:填空题
(10分)I、按要求书写热化学方程式:
(1)下图为N2(g)和02(g)生成NO(g)过程中的能量变化:

NO(g)分解生成N2(g)和O2(g)的热化学方程式为___________________;
(2)化合物AX3和单质X2在一定条件下反应可生成化合物AX5。己知AX3的熔点和沸点分别为为-93.6℃和76℃,AX5的熔点为167℃,室温时,AX3与气体X2反应生成1mol AX5,放出热量123.8kJ.该反应的热化学方程是为______.
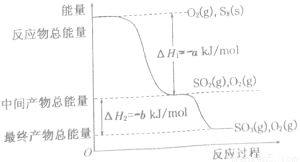
II、已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如下图所示:

在一定条件下,S8(s)和O2(g)发生反应依次转化为S02(g)和S03(g)。反应过程和能量关系可用下图简单表示(图中的△H表示生成1mol产物的数据)。
(3)写出表示S8燃烧热的热化学方程式_________________。
(4)写出SO3分解生成SO2和O2的热化学方程式___________________。
(5)若已知S-O键的键能为dkJ/mol,O=O键的键能为ekJ/mol,则S8分子中S-S键的键能为_______kJ/mol。
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:实验题
(10分)研究催化剂对化学反应有重要意义。为探究催化剂对双氧水分解的催化效果,某研究小组做了如下实验:

(1)甲同学欲用上图所示实验来证明MnO2是H2O2分解反应的催化剂。该实验______ (填“能”或“不能”)达到目的,原因是_____________。(若能,不必回答原因)
(2)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10mL5%H2O2)

由此得到的结论是__________ ,设计实验Ⅲ的目的是__________。
(3)在上述实验过程中,分别检测出溶液中有二价铁生成,查阅资料得知:将作为催化剂的FeCl3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的化学方程式分别是__________和__________(按反应发生的顺序写)。
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:填空题
(10分)下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
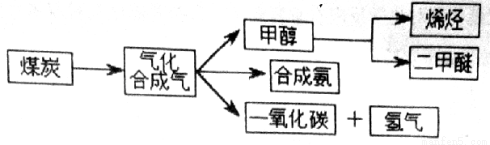
I.已知该产业链中某反应的平衡表达式为: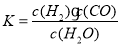 ,它所对应反应的化学方程式___________________(要注明物质的状态).
,它所对应反应的化学方程式___________________(要注明物质的状态).
II、二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0MPa,温度230~280 ℃)进行下列反应:
CO(g)+2H2(g) CH3OH(g) △H1=一90.7kJ·mol-1
CH3OH(g) △H1=一90.7kJ·mol-1
②2CH3OH(g)  CH3OCH3(g)+H2O(g) △H2=一23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=一23.5 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
(1)催化反应室中总反应的热化学方程式为______________。830℃时反应③的K=1.0 ,则在催化反应室中反应③的K___1.0 (填“> ”、“< ”或“=”)。
(2)在某温度下,若反应①的起始浓度分别为,c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50% ,则5 min 内CO的平均反应速率为______;若反应物的起始浓度分别为:c(CO)=4mol/L,c(H2)=amol/L,达到平衡后,c(CH3OH)=2mol/L,a=______mol/L。
查看答案和解析>>
科目: 来源:2016-2017学年河北冀州市高二上开学调研化学卷(解析版) 题型:填空题
(10分)反应aA(g)+bB(g) cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
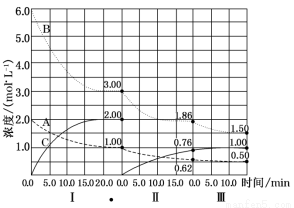
(1)反应的化学方程式中,a:b:c为_______;
(2)由第一次平衡到第二次平衡,改变的条件是__________;
(3) 由第二次平衡到第三次平衡,改变的条件是_________;
(4)第II阶段B的平衡转化率aII(B)=_______________;
(5)三次平衡时平衡常数KI、KII、KIII的大小顺序为_______________。
查看答案和解析>>
科目: 来源:2016-2017学年河北正定中学高二上开学考试化学卷(解析版) 题型:选择题
化学与生活密切相关,下列说法不正确的是( )
A.二氧化硫可广泛用于食品的增白 B.葡萄糖可用于补钙药物的合成
C.聚乙烯塑料制品可用于食品的包装 D.次氯酸钠溶液可用于消毒杀菌
查看答案和解析>>
科目: 来源:2016-2017学年河北正定中学高二上开学考试化学卷(解析版) 题型:选择题
下列操作中仪器使用不正确的是( )
A. 容量瓶未经干燥不能用来配制溶液 B. 用铁坩埚灼烧烧碱
C. 中和热的测定实验中用环形玻璃棒搅拌 D. 加热蒸发皿时不用石棉网
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com