
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:

下列有关判断中不正确的是( )
A.溶液A和溶液B均可以是盐酸或NaOH溶液
B.实验室中方案Ⅱ更便于实施
C.若溶液B选用浓硝酸,测得铜的质量分数偏大
D.方案一可能产生氢气,方案二可能剩余铜
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
24ml浓度为0.05mol·L-1的Na2SO3溶液(已知硫元素最高价为+6价),恰好与20mL 浓度为0.02mol•L-1 的K2Cr2O7(Cr元素最高价为+6价) 溶液完全反应,则元素Cr在被还原的产物中的化合价是
A.+6 B.+3 C.+2 D.0
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是
(甲)XO3n-+Xn-+H+→X单质+H2O(未配平);(乙)Mm++mOH-=M(OH)m↓
①若n=1,则XO3n-中X元素为+5价,X位于周期表第VA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m
A. ①③ B. ④⑤ C. ①② D. ②③
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列离子方程式的书写及评价,均合理的是
选项 | 离子方程式 | 评价 |
A | 将2molCl2通入到含1mol FeI2的溶液中: 2Fe2++2I-+2Cl2 = 2Fe3++4Cl-+I2 | 正确:Cl2过量,可将Fe2+ 、I-均氧化 |
B | Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++HCO3-+OH-= MgCO3↓+ H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入到NaClO溶液中: SO2 + H2O + ClO- = HClO+HSO3- | 正确; 说明酸性:H2SO3强于HClO |
D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合: 2AlO2- +5H+ =Al3+ +Al(OH)3↓+ H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2:3 |
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
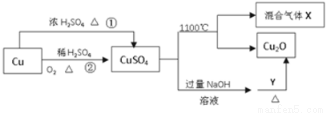
A.相对于途径①,途径②更好地体现了绿色化学思想
B.Y可以是葡萄糖溶液
C.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol
D.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
将1.28g Cu投入一定量的浓HNO3溶液中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下的气体448mL,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入的氧气的体积为
A.112 mL B.224 mL C.336 mL D.448 mL
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:选择题
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验:

下列说法中正确的是
A.步骤I中减少的3g固体一定是混合物
B.步骤II中质量减少的物质一定是Cu
C.根据步骤I、II可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
D.根据上述步骤II可以得出m(Fe2O3):m(Cu)=1:1
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:填空题
(14分)下图由短周期元素形成的物质之间的转化关系,其中A、D、L为单质,其他为化合物。其中化合物I、J、K中含有两种相同的元素,G和I的反应⑤是一种重要化工生产中的主要反应之一。B常温下为液态化合物,F是一种直线型的非极性气体分子。
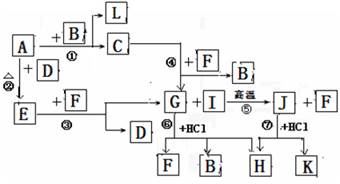
试回答下列有关问题:
(1)以上7个化学反应属于同种元素自身氧化还原反应的是 ;(用编号①→⑦填写)
(2)在G、J、H中含有相同的元素是 (填元素名称);
(3)J的水溶液和F______(填“能”或”否”)发生反应,其理由是 ;
(4)写出电解溶液H的离子反应方程式 ;
(5)反应⑤的化学方程式是 ;
(6)写出J的两种常见用途 、 。
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:实验题
(10分)以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
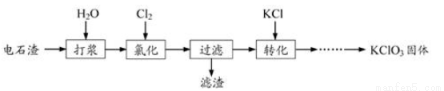
(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为 ;
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为
6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O 氯化完成后过滤。
①滤渣的主要成分为 (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2] 1∶5(填“>”、“<”或“=”)。
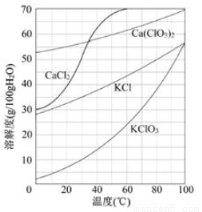
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100g·L-1,从该溶液中尽可能多地析出KClO3固体的方法是 。
查看答案和解析>>
科目: 来源:2017届黑龙江省高三上学期开学考试化学试卷(解析版) 题型:推断题
(12分)1000ml某待测溶液中除含有0.2mol·L-1的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |
现进行如下实验操作(每次实验所加试剂均过量):
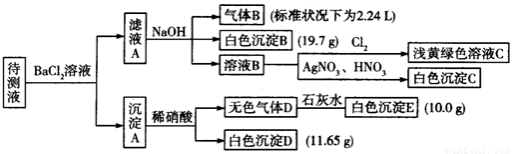
(1)写出生成白色沉淀B的离子方程式: 。
(2)待测液中肯定不存在的阳离子是 。
(3)若无色气体D是单一气体:判断原溶液中K+是否存在 (填是或否),若存在,求其物质的量浓度的最小值,若不存在,请说明理由: 。
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是 。
②沉淀A中能与稀硝酸反应的成分是 (写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com