
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
某兴趣小组设计如图装置进行氯气与金属钠的反应,先将钠预热,在钠熔融成小球时,撤火,并通入氯气即发生反应,下列叙述中错误的是( )

A.钠在氯气中燃烧产生黄色的火焰
B.反应产生的大量白烟是氯化钠固体
C.棉球①的作用是吸收过量氯气防止产生污染
D.棉球②变蓝色则证明氯气已被碱液完全吸收
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
缬氨霉素(valinomycin)是一种脂溶性的抗生素,是由12个分子组成的环状化合物,它的结构简式如图所示,有关说法正确的是
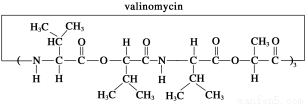
A.缬氨霉素是一种蛋白质
B.缬氨霉素完全水解可得到四种氨基酸
C.缬氨霉素完全水解后的产物中有两种产物互为同系物
D.缬氨霉素完全水解,其中一种产物与甘油互为同分异构体
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol<n(CO2)≤0.015时发生的反应是:
2NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
某学生做如下实验:第一步,在淀粉?KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列对实验原理的解释和所得结论错误的是( )
A. 蓝色逐渐消失的原因是Na2SO3溶液具有漂白性
B. 第一步反应的离子方程式ClO-+2I-+2H+===I2+Cl-+H2O
C. 淀粉?KI溶液变蓝是因为I-被氧化为I2,I2使淀粉变蓝色
D. 微粒的氧化性由强到弱的顺序是ClO->I2>SO
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
某无色溶液中可能含有Na+、K+、NH4+、Mg2+、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种,离子浓度都为0.1mol·L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
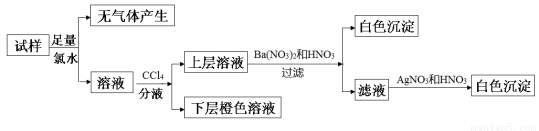
则关于原溶液的判断不正确的是
A.若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响
B.无法确定原溶液中是否存在Cl-
C.肯定存在的离子是SO32-、Br-,是否存在Na+、K+需要通过焰色反应来确定
D.肯定不存在的离子是Mg2+、Cu2+、SO42-、CO32-,是否含NH4+另需实验验证
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,则下列有关说法中不正确的是( )

A.还原性:I->Fe2+>Br-
B.线段AB表示Fe2+被氯气氧化
C.线段BC表示生成4 mol Fe3+
D.原溶液中n(Br-)=6 mol
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:选择题
取一定质量的均匀固体混合物Cu、Cu2O和CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g ,另一份中加入500ml稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为
A.3.2mol/L B.3.6mol/L C.4.0mol/L D.无法判断
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:实验题
(1)写出铁与水蒸气反应的化学方程式______________________________。
(2)已知Cu2S可以和硝酸反应,请配平下列化学反应方程式:
Cu2S+ HNO3 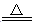 CuSO4 + Cu(NO3)2+ NO↑+
CuSO4 + Cu(NO3)2+ NO↑+
(3)某校兴趣小组欲测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g,通过计算确定此合金的组成为 (填化学式)。
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:实验题
(10分)
(1)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①Fe2O3(Al2O3) ②NaHCO3(Na2CO3)
③Cl2 (HCl) ④SiO2 (Fe2O3)
(2)将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应(容器不参与反应)。试判断下列情况下,溶液中存在的金属离子和金属单质。
①若铁粉有剩余,则容器中不可能有的离子是________________;铜单质________(填“一定”或“可能”)存在。
②若氯化铜有剩余,则容器中还可能有的离子为________;铜单质__________(填“一定”或“可能”)存在。
③若氯化铁和氯化铜都有剩余,则容器中不可能有的单质是______,Fe2+_______(填“一定”或“可能”)存在。
查看答案和解析>>
科目: 来源:2017届江西省高三7月暑期阶段性测试化学试卷(解析版) 题型:实验题
(12分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。

(1)B中反应的离子方程式是_ ___。
(2)A中溶液变红的原因是__ __。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在 。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是SCN-与Cl2发生了反应。
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN-的电子式为
①甲同学认为SCN-中碳元素没有被氧化,理由是 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是 。
③通过实验证明了SCN-中氮元素转化为NO3-。
④若SCN-与Cl2反应生成1 mol CO2,则转移电子的物质的量是 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com