
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:选择题
下列叙述中,正确的是( )
A.醛和酮是不同类的同分异构体,二者的化学性质相似
B.能发生银镜反应的物质是醛,1mol醛与银氨溶液反应只能还原出2mol Ag
C.醛类化合物既能发生氧化反应,又能发生还原反应
D.丙醛、丙酮、丙酸均能与氢气在催化剂作用下发生加成反应
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:选择题
等物质的量下列物质中,完全燃烧时消耗O2最少的是( )
A.甲烷 B.苯
C.乙酸丙酯 D.乙二醛(OHC﹣CHO)
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:选择题
将29.5g乙烷和乙烯的混合气体通入足量的溴水后,溴水质量增加7g,则混合气体中乙烯的体积分数是( )
A.21% B.25% C.30% D.35%
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:选择题
把含硫酸铵和硝酸铵的混合液a L分成两等份.一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42﹣完全沉淀,则原溶液中NO3﹣的物质的量浓度为( )
A. B.
B. C.
C.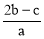 D.
D.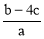
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:计算题
已知在某温度T℃时,某稀硫酸和盐酸混合液中,c(H+)=10﹣amol•L﹣1,c(OH﹣)=10﹣bmol•L﹣1,已知a+b=12.向20mL该混合酸溶液中逐滴加 入pH=11Ba(OH)2溶液,生成BaSO4的质量与加入的Ba(OH)2溶液体积关系如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
入pH=11Ba(OH)2溶液,生成BaSO4的质量与加入的Ba(OH)2溶液体积关系如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
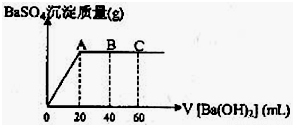
(1)最初混合酸溶液中c(HCl)= ;
(2)图中 点BaSO4就已被完全沉淀,质量为 克;
(3)B点pH= (第(3)步要求写出计算过程)(已知lg3=0.48)。
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:计算题
过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6H2O CaO2·8H2O
CaO2·8H2O
反应时通常加入过量的Ca(OH)2,其目的是_____________。
(2)向池塘水中加入一定量的CaO2·8H2O后,池塘水中浓度增加的离子有____________(填序号)。
A.Ca2+ B.H+ C.CO32- D.OH-
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
O2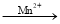 MnO(OH)2
MnO(OH)2 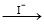 I2
I2 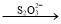 S4O62-
S4O62-
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:_____________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水样的溶解氧,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶 解氧(用mg·L-1表示),写出计算过程。
解氧(用mg·L-1表示),写出计算过程。
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:填空题
下表是元素周期表的一部分,请按要求回答有关问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 |
|
|
| ① | ② |
| ③ |
|
3 |
| ④ | ⑤ |
|
| ⑥ | ⑦ | ⑧ |
4 | ⑨ |
|
|
|
|
| ⑩ |
|
(1)表中化学性质最不活泼的元素的原子结构示意图为: ;
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨的最高价氧化物对应的水化物反应的离子方程式: ;
(3)元素④与元素⑦形成的化合物中的化学键类型是 ,写出该化合物的电子式: ;
(4)①②⑥⑦四种元素的最高价氧化物对应的水化物中酸性最弱的是 (填化学式);
(5)元素③与元素⑩两者核电荷数之差是 ;
(6)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的元素是: (填序号);
(7)④⑤⑥⑦四种元素的简单离子的半径由大到小的顺序为: (填化学式).
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:实验题
钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如图(废料中含有Al、Li、Co2O3和Fe2O3等物质).
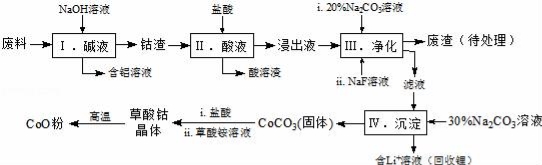
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表.
Fe3+ | Co2+ |
| Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | ﹣0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式: 。
(2)步骤Ⅲ中 Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过 ;废渣中的主要成分除了LiF外,还有 。
(3)NaF 与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是 。
(4)在空气中加热5.49g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表.已知:M(CoC2O4·2H2O)=183g/mol
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~ | 2.25 |
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是 。温度高于890℃时,固体产物发生分解反应,固体产物为 。
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:填空题
化学电池的研究一直是化学工作者研究的热点之一.
Ⅰ.美国科学家S•鲁宾成功开发锌汞纽扣式电池,以锌和氧化汞为电极材料,氢氧化钾溶液为电解液的原电池,有效地解决电池使用寿命短,易发生漏液等问题.电池总反应为:Zn+HgO═ZnO+Hg。
(1)该电池的正极反应式为 。
(2)含汞电池生产企业的污水中会含有一定量的+2价的汞离子,通常采用处理成本较低的硫化物沉淀法,即向污水中投入一定 量的硫化钠,反应的离子方程式为 。
量的硫化钠,反应的离子方程式为 。
(3)该方法的缺点是产物的颗粒比较小,大部分悬浮于污水中,通常采用投入一定量的明矾晶体进行后续处理,请解释其原因 。
Ⅱ.锂离子电池由于轻便、比能量大等优点,成为当今社会最为常见的电池.其中的重要材料磷酸亚铁锂(LiFePO4)通常按照下列流程进行生产:
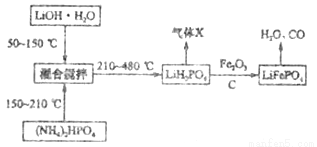
请回答下列问题:
(4)生产过程中“混合搅拌”的目的是 。气体X的化学式为 。
(5)请写出一定条件下由LiH2PO4生成LiFePO4的化学方程式 ,当生成1mol磷酸亚铁锂时,转移的电子数目为 。
(6)生成LiFePO4的过程可能产生一种杂质对电池有致命的影响,则该杂质可能为 。
查看答案和解析>>
科目: 来源:2016-2017学年广东省高二上第一次月考化学卷(解析版) 题型:填空题
工业上通过电解MnSO4和ZnSO4制取Zn和MnO2,原料为软锰矿和闪锌矿,软锰矿中含MnO2约a%,SiO2约20%,Al2O3约4%,其余为水分,闪锌矿中含ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分。
I.(1)为了测量软锰矿中MnO2含量的测定,现将14.5g软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取25.00ml该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用0.1000mol•L﹣1的标准Na2S2O3溶液滴定,消耗标准液50.00ml,则软锰矿中MnO2含量 。(已知:2KI+2H2SO4+MnO2=I2+2H2O+MnSO4+K2SO4; I2+2S2O32﹣=2I﹣+S4O62﹣)
Ⅱ.研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示。

请回答下列问题:
(2)反应I的滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等.试完成反应I中生成CuSO4和MnSO4的化学方程MnO2+CuS+ = + +CuSO4+MnSO4。
(3)反应Ⅱ加入适量锌的作用是 ;如果锌过量,还会进一步发生反应的离子方程式为 。
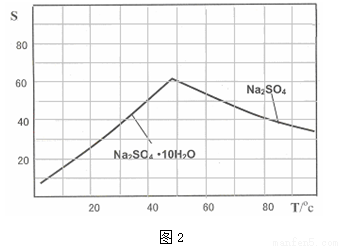
(4)图2是Na2SO4和Na2SO4•10H2O的溶解度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶→ →用乙醇洗涤→干燥.用乙醇洗涤而不用水洗的原因是 。
(5)用惰性电极电解MnSO4和ZnSO4制得Zn和MnO2的总反应是: 。
(6)本工艺可以循环利用的物质除MnO2、MnCO3、ZnCO3以外,还有 (写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com