
科目: 来源:同步题 题型:填空题
查看答案和解析>>
科目: 来源:0112 期中题 题型:填空题

查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
科目: 来源:0116 同步题 题型:填空题
硝化甘油(C3H5N3O9)分解时产物为N2、CO2、O2和液态水,它的分解反应的化学方程式是________________________。已知20℃时,22.7g硝化甘油分解放出的热量为154kJ,则每生成1mol气体伴随放出的热量为____________kJ。
查看答案和解析>>
科目: 来源:专项题 题型:单选题
[ ]
查看答案和解析>>
科目: 来源:浙江省期中题 题型:单选题

查看答案和解析>>
科目: 来源:浙江省期中题 题型:填空题
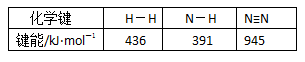
 2NH3(g) ;△H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:_______________(注明“+“-”)。
2NH3(g) ;△H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:_______________(注明“+“-”)。 CH3OH(g);△H =-90.8 kJ·mol-1
CH3OH(g);△H =-90.8 kJ·mol-1  CH3OCH3(g) + H2O(g);△H=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);△H=-23.5 kJ·mol-1  CO2(g) + H2(g);△H=-41.3 kJ·mol-1
CO2(g) + H2(g);△H=-41.3 kJ·mol-1  CH3OCH3(g) + CO2 (g)的△H=____________。
CH3OCH3(g) + CO2 (g)的△H=____________。查看答案和解析>>
科目: 来源:江西省期中题 题型:填空题
查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:单选题
查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com