
科目: 来源:2017届云南省高三第一次摸底化学试卷(解析版) 题型:填空题
[化学—选修2:化学与技术]
海水占地球总储水量的97.2﹪。若把海水淡化和化工生产结合起来,既能解决淡水资源缺乏的问题,又能充分利用海洋资源。
下图是利用海水资源进行化工生产的部分工艺流程示意图:

(1)该工艺流程示意图中包含了 、 (填化学工业的名称)。
(2)在流程Ⅰ中,欲除去粗盐中含有的Ca2+、Mg2+、SO42+等离子,需将粗盐溶解后,按顺序加入药品进行沉淀、过滤等。加入药品和操作的顺序可以是 (填字母)。
A.Na2CO3、NaOH、 BaCl2、过滤、盐酸
B.NaOH、 BaCl2、 Na2CO3、过滤、盐酸
C.NaOH、 Na2CO3、 BaCl2、过滤、盐酸
D.BaCl2、Na2CO3、 NaOH、 过滤、盐酸
(3)流程Ⅱ中,通电开始后,阳极区产生的气体是 (填化学式),阴极附近溶液pH会 (填“增大”、“减小”或“不变”)。
(4)流程Ⅲ中,通过相应化学反应可以得到NaHCO3晶体。下图为NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲线,其中能表示NaHCO3溶解度曲线的是 ,生成NaHCO3晶体的化学反应方程式是 。

(5)流程Ⅳ中,所得纯碱常含有少量可溶性杂质,常用的提纯方法是 (填名称),通过该法提纯后得到纯净的Na2CO3·10H2O,Na2CO3·10H2O脱水得到无水碳酸钠。
已知:Na2CO3·H2O(s)=Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
把脱水过程产生的气态水完全液化释放的热能全部用于生产Na2CO3所需的能耗(不考虑能量损失),若生产1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)= H2O(l) △H= 。
查看答案和解析>>
科目: 来源:2017届云南省高三第一次摸底化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质]
A、B、C、D、E是前四周期原子序数依次增大的五种元素。A元素原子的核外电子等于其电子层数;B元素基态原子有三个能级电子数相同;A和D可形成两种常见液态化合物甲、乙,其原子数之比分别为1:1,2:1;E元素原子的K、L层电子数之和等于其M、N层电子数之和。回答下列问题(涉及元素用相应化学符号表示):
(1)B、C、D三种元素中电负性最大的元素其基态原子的电子排布式为 。
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用 形象化描述。在B的基态原子中,核外存在 对自旋相反的电子。
(3)由E和D形成的晶胞如图1所示,晶体中E2+周围等距且最近的E2+有 个;ED的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色反应,焰色反应的原理是 。E和B可形成的晶体的晶胞结构与NaCl晶体的相似(如图2所示),但该晶体中含有的哑铃形B22-的存在,使晶胞沿一个方向拉长。晶体中E2+的配位数为_______________;该化合物的化学式为 。

(4)用高能射线照射液态化合物乙时,一个乙分子能释放出一个电子,同时产生一种阳离子。
①释放出来的电子可以被若干乙分子形成的“网”捕获,乙分子间能形成“网”的原因是 。
②由乙分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式 。
查看答案和解析>>
科目: 来源:2017届云南省高三第一次摸底化学试卷(解析版) 题型:推断题
[化学—选修5:有机化学基础]
甲基丁炔醇(简写为MB),用作医药和香料中间体,酸蚀抑制剂、镀镍或镀铜的上光剂等。MB的一种人工合成路线设计如下:
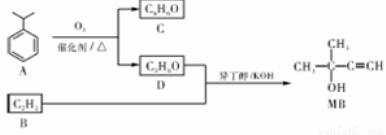
已知:①C的溶液中滴加FeCl3溶液后显紫色
②D的核磁共振氢谱显示只有一种化学环境的氢
③R2COR2+HC=CR3 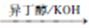
回答下列问题:
(1)A氧化时,理论上生成C和D的物质的量之比为 。
(2)B、C的结构简式分别为 、 ,D的官能团名称为 。
(3)B+D→MB的反应类型为 ;用系统命名法,MB的化学名称为 。
(4)B+D→MB的反应时间不宜超过两个小时,否则MB与D发生二次反应使产率降低,MB与D反应的化学方程式为 。
(5)某有机物E和A的芳香烃异构体,E的可能结构共有 种(不考虑立体异构),写出其中只有两种不同化学环境的氢,数目比为3:1的异构体的结构简式 。
(6)已知:端炔化合物在一定条件下可发生偶联反应,如:
2R-C≡CH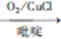 R-C≡C-C≡C-R
R-C≡C-C≡C-R
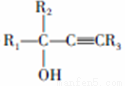
写出由2-丙醇和乙炔为初始原料(其他有机溶剂、无机试剂任选)合成2,7-二甲基-3,5-辛二炔-2,7-二醇(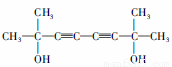 ,医药中间体,材料中间体)的合成路线。
,医药中间体,材料中间体)的合成路线。
合成路线流程图示例如下:

查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
下列有关放热反应、吸热反应的说法不正确的是
A.吸热反应的发生都需要加热,放热反应在常温下一定容易发生
B.若某反应正向进行时为放热反应,则该反应逆向进行时必为吸热反应
C.由“C(石墨)=C(金刚石)是吸热反应”可知石墨比金刚石稳定
D.不管是吸热反应还是放热反应,升高温度,反应速率均增大
查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
己知反应A+B=C+D的能量变化如图所示,下列说法正确的是
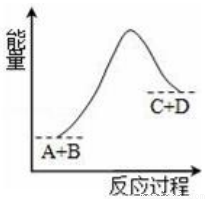
A.该反应为放热反应 B.该反应为吸热反应
C.反应物的总能量高于生成物的总能量 D.该反应只有在加热条件下才能进行
查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
己知:①CH3OH(g) +3/2O2(g)=CO2(g)+2H2O(g) △H=-a kJ·mol-l
②CH4(g) +2O2 (g) =CO2 (g) +2H2O(g) △H=-b kJ·mol-l
⑧CH4(g) +2O2 (g) =CO2 (g) +2H2O(1) △H=-c kJ·mol-l
则下列叙述正确的是
A.由上述热化学方程式可知b>c
B.甲烷的燃烧热为bkJ/mol
C.2CH3OH (g) =2CH4(g)+O2(g) △H=2(b-a) kJ·mol-l
D.当甲醇和甲烷物质的量之比为1:2时,其完全燃烧生成CO2和H2O (1)时,放出的热量为Q kJ,则该混合物中甲醇的物质的量为Q/(a+2b) mol
查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.强电解质都易溶于水,所以BaSO4是弱电解质
B.一定条件下醋酸溶液的导电能力可能比稀硫酸强
C.SO2的水溶液能导电,所以SO2是电解质
D.金刚石不导电,因此金刚石是非电解质
查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol.L-l的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是
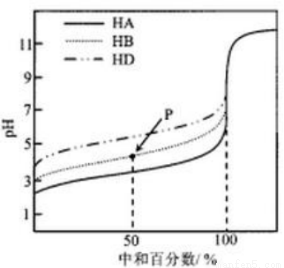
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA) +c (HB) +c (HD) =c (OH-) -c (H+)
查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的,它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,下列判断正确的是
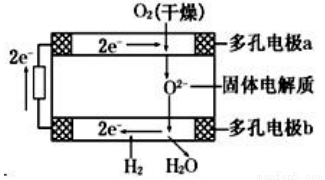
A.有O2放电的a极为电池的负极
B.O2-移向电池的正极
C.b极对应的电极反应为2H2- 4e-+2O2-=2H2O
D.a极对应的电极反应为O2+2H2O+4e-=4OH-
查看答案和解析>>
科目: 来源:2016-2017学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值小于HX溶液的pH改变值
B.在NH3·H2O和NH4Cl浓度均为0.1 mol·L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变
C.在NaH2PO4水溶液中存在关系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-)
D.沉淀溶解平衡AgI Ag++I-的平衡常数为8.5×10-17,说明难溶盐AgI是弱电解质
Ag++I-的平衡常数为8.5×10-17,说明难溶盐AgI是弱电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com