
科目: 来源:2017届贵州省高三一模理综化学试卷(解析版) 题型:填空题
钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C 2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C
2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C TiCl4+2CO
TiCl4+2CO
将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg Ti+2MgCl2
Ti+2MgCl2
MgCl2和过量Mg用稀盐酸溶解后得海绵状钛,再在真空熔化铸成钛锭。请回答下列问题:
(1)基态钛原子的价电子排布式为__________________。
(2)与CO互为等电子体的离子为__________(填化学式)。
(3)在CH2Cl2、C6H6、CO2、C2H4中,碳原子采取sp杂化的分子有__________ 。
(4) C60用做比金属及其合金更为有效的新型吸氢材料,其分子结构中每一个C原子皆为SP2杂化,含多个σ键和π键,36gC60最多可以吸收标准状况下的氢气____________L。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是__________________ ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 _______________ 。
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如下图所示,则其中Ti4+的配位数为__________。

查看答案和解析>>
科目: 来源:2017届贵州省高三一模理综化学试卷(解析版) 题型:推断题
(有机化学基础)分子式为C12H14O2的有机物F广泛用于制备香精的调香剂。为了合成该有机物,某实验室的科技人员设计了下列合成路线。
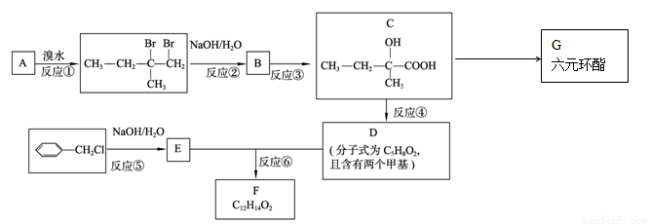 试回答下列问题:
试回答下列问题:
(1)A物质名称为(系统命名) 。
(2)合成路线中反应③所属反应类型为 。
(3)有机物G的结构简式为 。
(4)有机物D中所含官能团的名称为 。
(5)关于有机物C,下列说法正确的是( )
A.等物质的量的C分别与足量的金属钠和NaHCO3反应,后者产生气体多
B.一定条件下,有机物C能通过缩聚反应形成高分子化合物
C.1molC完全燃烧生成CO2和H2O,消耗的氧气的物质的量为6mol
D.有机物C中的所有碳原子可能在同一平面上
(6)反应⑥的化学反应方程式为 。
(7)F有多种同分异构体,请写出符合下列条件的所有同分异构体的结构简式:①属于芳香族化合物,且含有与F相同的官能团;②苯环上有两个取代基,且苯环上的一氯代物只有两种;③其中一个取代基为-CH2COOCH3; 。
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
下列化学事实及其解释都正确的是
A.滴有酚酞的碳酸氢钠溶液显红色,微热后红色加深,是因为碳酸氢钠分解生成了碳酸钠
B.用洁净的玻璃管向包有过氧化钠的脱脂棉吹气,脱脂棉燃烧,说明二氧化碳、水与过氧化钠的反应是放热反应
C.向溴水中滴入植物油,振荡后油层显无色,说明溴不溶于油脂
D.粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
已知:碘单质能与I-反应成I3-,并在溶液中建立如下平衡:I2+I I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。某同学为测定上述平衡体系中C(I2),采用如下方法:取V1mL平衡混合溶液,用cmol•L-1的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗V2mL的Na2S2O3溶液。根据V1、V2和c可求得c(I2)。下列对该同学设计方案的分析,正确的是
I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),就可求得该反应的平衡常数。某同学为测定上述平衡体系中C(I2),采用如下方法:取V1mL平衡混合溶液,用cmol•L-1的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗V2mL的Na2S2O3溶液。根据V1、V2和c可求得c(I2)。下列对该同学设计方案的分析,正确的是
A.方案可行,能准确测定溶液中的c(I2)
B.方案可行,可采用淀粉做该滴定反应的指示剂
C.不可行,只能测得溶液中c(I2)与c(I3-)之和
D.不可行,因为I-能与Na2S2O3溶液反应
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
0.1mol金属锡跟100mL12mol/LHNO3共热一段时间,完全反应后放出气体0.4mol,测定溶液c(H+)=8mol/L,溶液体积仍为100mL。由此推断氧化产物可能是
A.Sn(NO3)2 B.Sn(NO3)4
C.SnO2•4H2O D.Sn(NO3)2和Sn(NO3)4
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
CO2+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | H2O/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是
A.反应在t1min内的平均速率为v(H2)=0.40/t1 mol•L-1•mim-1
B.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,0.4molH2,则v(正)>v(逆)
D.保持其他条件不变,起始时向容器中充入0.60mol CO和1.20mol H2O,到达平衡时n(CO2)=0.40mol
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
分子中碳与氢元素的质量比为21:4的烃中,主链上有5个碳原子的结构共有几种
A.5 B.6 C.4 D.3
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
常温下,向等体积、等物质的量浓度的盐酸、醋酸溶液中分别滴入0.1mol/LNaOH溶液,测得溶液的pH与NaOH溶液体积的关系如图所示。下列说法错误的是

A.图中曲线①表示NaOH溶液滴定盐酸时的pH变化
B.酸溶液的体积均为10 mL
C.a点:c(CH3COOH)>c(CH3COO-)
D.a点:c(H+)+c(Na+)=c(OH-)+c(CH3COO-)
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:选择题
在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是
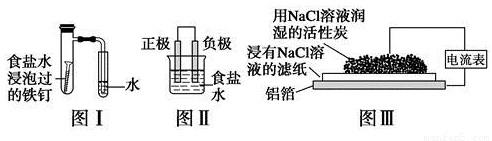
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目: 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:实验题
某学生对Na2SO3与AgNO3在不同pH下的反应进行探究。
(1)测得Na2SO3溶液pH=11,AgNO3溶液pH=5,二者水解的离子分别是 。
(2)调节pH,实验记录如下:
实验 | pH | 现象 |
A | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
B | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
C | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
查阅资料得知:
Ⅰ.Ag2SO3:白色,难溶于水,溶于过量Na2SO3的溶液
Ⅱ.Ag2O:棕黑色,不溶于水,能和酸反应
①推测a中白色沉淀为Ag2SO3,离子方程式是 。
②推测a中白色沉淀为Ag2SO4,推测的依据是 。
(3)取b、c中白色沉淀,置于Na2SO3溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是Ag2SO4,实验方法是:另取Ag2SO4固体置于 溶液中,未溶解。
(4)将c中X滤出、洗净,为确认其组成,实验如下:
Ⅰ.向X中滴加稀盐酸,无明显变化
Ⅱ.向X中加入过量浓HNO3,产生红棕色气体
Ⅲ.用Ba(NO3)2溶液、BaCl2溶液检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀
①实验Ⅰ的目的是 。
②根据实验现象,分析X的性质和元素组成是 。
③Ⅱ中反应的化学方程式是 。
(5)该同学综合以上实验,分析产生X的原因,认为随着酸性的增强,还原性增强。通过进一步实验确认了这种可能性,实验如图所示:

①气体Y是 。
②白色沉淀转化为X的化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com