
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
某化合物由五种短周期元素组成,分别为X、Y、Z、W、R,原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是
A. Z与Y形成的化合物是工业上制取Z的原料
B. WY2可与酸反应,但不能与碱反应
C. 原子半径按X、Y、Z、R、W的顺序依次增大
D. 热稳定性 :X2R>X2Y
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列说法错误的是
A. 和CO2反应生成可降解聚合物
和CO2反应生成可降解聚合物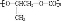 ,该反应符合绿色化学原则
,该反应符合绿色化学原则
B.正丁烷的二氯代物有5种(不考虑立体异构)
C.乙醇在铜催化下加热可脱氢生成乙醛,该反应属于氧化反应
D.淀粉、纤维素、麦芽糖均属于糖类,在一定条件下都可以水解得到葡萄糖
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列三种烃的立体结构如图示:
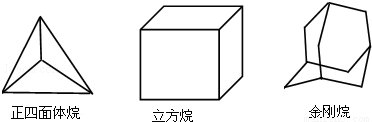
则这三种烃的二氯取代产物的同分异构体数目分别是
A.2,4,8 B.2,4,6 C.1,3,6 D.1,3,8
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列说法正确的是

A.图①中△H2=△H1+△H3
B.图②在催化剂条件下,反应的活化能等于E1+E2
C.图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲 线
线
D.图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
中关村“创客19”实验室模拟光合作用的电化学实验装置如右图所示,该装置能将H2O和CO2转化为O2和葡萄糖(C6H12O6)。下列说法 正确的是
正确的是
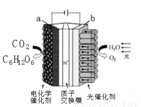
A.该装置是新型化学电源装置
B.该装置工作时,H+从a极区向b极区迁移
C.每生成1 mol O2,有44 g CO2被还原
D.a 电极的反应为: 6CO2 + 24H+-24e-= C6H12O6 +6 H2 O
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g) +Y(g) 3Z(g) △H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g) △H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是

A.升高温度,平衡常数增大
B.W点X的正反应速率小于M点X的正反应速率
C.Q点时,Y的转化率最小
D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列说法不正确的是
A.对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变 值大于HX溶液的pH改变值
值大于HX溶液的pH改变值
B.在NH3·H2O和NH4Cl浓度均为0.1 mol·L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变
C.在NaH2PO4水溶液中存在关系:c(H3PO4) + c(H+) = c(HPO42-) + c(PO43-) + c(OH-)
D.沉淀溶解平衡AgI  Ag+ + I- 的平衡常数为8.5×10-17,不能说明难溶盐AgI是弱电解质
Ag+ + I- 的平衡常数为8.5×10-17,不能说明难溶盐AgI是弱电解质
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:填空题
大苏打(Na2S2O3·5H2O)、苏打、小苏打被称为“三苏”,它们在生 活、生产中用途广泛。
活、生产中用途广泛。
(1)工业上,将苏打和硫化钠以1:2的物质的量之比配成溶液,再通入SO2气体,可制得Na2S2O3,同时放出CO2。写出该反应的化学方程式 。硫化钠溶液在空气中久置,会生成淡黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的化学式 。
(2)Na2S2O3标准液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高,用离子方程式表示其原因 。
(3)工业上用大苏打溶液吸收工业废气中的氯气,其氧化产物为SO42-,写出离子方程式 。
(4)工业上常用苏打和盐酸除去锅炉中水垢中的硫酸钙。先用饱和苏打溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是 。(并用离子方程式表示)
(5)在密闭的容器中投入一定量的Na2O2和NaHCO3固体,在300℃下充分反应。若残留固体为纯净物,则起始时n(NaHCO3):n(Na2O2)满足的条件是 。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:实验题
磷酸亚铁[Fe3(PO4)2·8H2O]为白蓝色晶体,溶于强酸,不溶于水、醋酸和乙醇。主要用于制造磷酸铁锂电池。实验室制备磷酸亚铁的装置示意图、
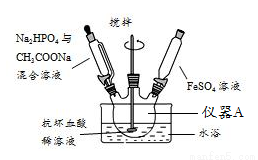
反应和实验步骤如下。主要反应为:
3FeSO4+2Na2HPO4+2CH3COONa+8H2O=Fe3(PO4)2·8H2O↓+3Na2SO4+2CH3COOH
实验步骤:①在仪器A中先加入抗坏血酸(C6H8O6)稀溶液作底液②向仪器A中,滴入Na2HPO4与CH3COONa混合溶液至pH=4 ③滴入 15.2克FeSO4溶液,最终维持pH=6,充分反应后,静置④进行操作a,干燥得到的磷酸亚铁12.8克。
15.2克FeSO4溶液,最终维持pH=6,充分反应后,静置④进行操作a,干燥得到的磷酸亚铁12.8克。
(1)仪器A的名称是 。
(2)实验中配制FeSO4溶液时,先要对蒸馏水进行的操作是 。
(3)实验中不是将三种溶液直接混合的原因是 ,反应时需不断搅拌,其目的是 。
(4)步骤④进行的操作a是 。
(5)检验磷酸亚铁粗产品中是否混有氢氧化铁杂质的方法是 。
(6)本实验的产率是 。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:填空题
氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用。
(1)液氨储氢是目前研究的重要课题。液氨的电离和水的电离相似,液氨中的氨也能发生电离:NH3+NH3 NH4++NH2-,其离子积常数为1.0×10-30。现将2.3克金属钠投入1.0 L 液氨中,待反应结束后,假设溶液体积不变,所得溶液中NH4+离子浓度为 。
NH4++NH2-,其离子积常数为1.0×10-30。现将2.3克金属钠投入1.0 L 液氨中,待反应结束后,假设溶液体积不变,所得溶液中NH4+离子浓度为 。
(2)用Pt电极对液氨进行电解可产生H2和N2,则阴极的电极反应式是 。
(3)用NH3催化还原NXOy可以消除氮氧化合物的污染。请写出氨气催化还原NO的化学方程式 。
(4)将一定量的N2和H2充入1L的密闭容器中,在500℃、2×107Pa下反应并达到平衡,测得N2为0.10 mol,H2为0.30 mol,NH3为0.10 mol,则H2的平衡转化率为 ;在该温度下的平衡常数K= 。

(5 )右图是某压强下,N2与H2按体积比1: 3投料时,反应混合物中氨的体积分数随温度的变化曲线。其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。则图中b点,v(正) v(逆)。(填“>”、
)右图是某压强下,N2与H2按体积比1: 3投料时,反应混合物中氨的体积分数随温度的变化曲线。其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。则图中b点,v(正) v(逆)。(填“>”、 “=”或“<”)
“=”或“<”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com