
科目: 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:选择题
分析下列反应在任何温度下均能自发进行的是( )
A.2N2(g)+O2(g)===2N2O(g)ΔH=+163 kJ·mol-1
B.Ag(s)+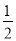 Cl2(g)===AgCl(s)ΔH=-127 kJ·mol-1
Cl2(g)===AgCl(s)ΔH=-127 kJ·mol-1
C.HgO(s)===Hg(l)+ O2(g) ΔH=+91 kJ·mol-1
O2(g) ΔH=+91 kJ·mol-1
D.H2O2(l)===  O2(g)+H2O(l) ΔH=-98 kJ·mol-1
O2(g)+H2O(l) ΔH=-98 kJ·mol-1
查看答案和解析>>
科目: 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:实验题
某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
实验 编号 | 0.01mol•L﹣1 酸性KMnO4溶液 | 0.1mol•L﹣1 H2C2O4溶液 | 水 | 1mol•L﹣1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
Ⅰ | 2mL | 2mL | 0 | 0 | 20 | 125 |
Ⅱ | V1 mL | V2 mL | 1mL | 0 | 20 | 320 |
Ⅲ | V3 mL | V4 mL | V5 mL | 0 | 50 | 30 |
Ⅳ | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
已知:反应的方程式(未配平):KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O
(1)实验记时方法是从溶液混合开始记时,至 时记时结束;
(2)实验I和Ⅱ研究浓度对反应速率的影响,实验Ⅰ和Ⅲ研究温度对反应速率的影响.则V1= V2= V3= V4= V5= ;
(3)从实验数据分析,实验I和IV研究 对反应的影响;
(4)请配平上面的化学方程式: KMnO4+ H2C2O4+ H2SO4= K2SO4+ MnSO4+ CO2↑+ H2O
查看答案和解析>>
科目: 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:填空题
(1)下列物质中,属于弱电解质的是(填序号,下同) ,属于非电解质是 .
①亚硫酸溶液 ②次氯酸钠 ③氯化氢气体  ④蔗糖 ⑤硫酸钡
④蔗糖 ⑤硫酸钡
⑥氨气 ⑦冰醋酸 ⑧硫酸氢钠固体 ⑨氢氧化铁 ⑩NO2
(2)写出下列物质在水中的电离方程式:硫酸氢钠: ;
(3)甲、乙两瓶氨水的浓度分别为1mol•L﹣1、0.1mol•L﹣1,则c(OH﹣)甲:c(OH﹣)乙 10 (填“大于”、“等于”或“小于”).
查看答案和解析>>
科目: 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:填空题
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________。
(2)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为______________。
(3)联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离方程式为:_________________。
查看答案和解析>>
科目: 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:填空题
丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的 热化学方程式如下:
热化学方程式如下:
①C3H6(g)+NH3(g)+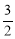 O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
②C3H6(g)+ O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol
两个反应在热力学上趋势均很大,其原因是________________;有利于提高丙烯腈平衡产率的反应条件是_____________;提高丙烯腈反应选择性的关键因素是___________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________________(填“是”或者“不是”)对应温度下的平衡
产率,判断理由是______________;高于460℃时,丙烯腈产率降低的可能原因是_____________(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大

(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为 ,理由是_________________。进料气氨、空气、丙烯的理论体积比约为________________。
查看答案和解析>>
科目: 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:填空题
硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)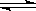 2SO3(g)△H<0
2SO3(g)△H<0
(1)如果2min内SO2的 浓度由6mol/L下降为2mol/L,那么,用O2浓度变化来表示的反应速率为 .
浓度由6mol/L下降为2mol/L,那么,用O2浓度变化来表示的反应速率为 .
(2)某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图1所示.根据图示回答下列问题:
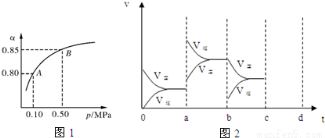
该反应的平衡常数的表达式为 平衡状态由A变到B时平衡常数K(A) K(B)(填“>”、“<”或“=”).
(2)此反应在恒温密闭的装置中进行,能充分说明此反应已达到平衡的标志是 (填字母).
A.接触室中气体的平均相对分子质量不再改变
B.接触室中SO2、O2、SO3的浓度相同
C.接触室中SO2、SO3的物质的量之比为2:1:2
D.接触室中压强不随时间变化而变化
(4)图2表示该反应在密闭容器中达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~ b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,请把反应速率变化情况画在c~d处.
查看答案和解析>>
科目: 来源:2016-2017年黑龙江佳木斯一中高一上9.10周练化学卷(解析版) 题型:选择题
下列有关物理量相应的单位错误的是( )
A.摩尔质量g/mol B.气体摩尔体积mol/L
C.溶解度g/100g D.物质的量mol
查看答案和解析>>
科目: 来源:2016-2017年黑龙江佳木斯一中高一上9.10周练化学卷(解析版) 题型:选择题
下列哪种物质所含原子数与0.2molH3PO4所含原子数相等( )
A.0.4molH2O2 B.0.2molH2SO4 C.0.7molNaCl D.0.3molHNO3
查看答案和解析>>
科目: 来源:2016-2017年黑龙江佳木斯一中高一上9.10周练化学卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列说法不正确的是( )
A.硫酸的摩尔质量以g/mol为单位时与NA磷酸分子的质量以g为单位时在数值上相等
B.NA个氮气分子和NA个氧气分子的质量比为7:8
C.3.2gO2所含的原子数约为0.2NA
D.常温、常压下,0.5NA个二氧化碳分子质量是44g
查看答案和解析>>
科目: 来源:2016-2017年黑龙江佳木斯一中高一上9.10周练化学卷(解析版) 题型:选择题
下列叙述中不正确的( )
A.1mol任何物质都含6.02×1023个原子
B.0.012kg12C约含有6.02×1023个碳原子
C.阿伏伽德罗常数个粒子的“集体”就是1mol
D.使用摩尔这一单位时必须指明微粒的种类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com