
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:选择题
某反应的反应过程中能量变化如右图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列说法错误的是( )
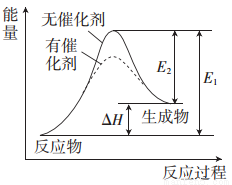
A.该反应为吸热反应
B.催化剂不能改变反应的焓变(△H)
C.催化剂能降低反应的活化能
D.逆反应的活化能大于正反应的活化能
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ·mol-l;
C3H8 (g)+5O2( g)=3CO2(g)+4H2O(1) △H =-2220 kJ·mol-l.
现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3847 kJ,则在混合气体中H2和C3H8的体积比是( )
A.2:1 B.3:1 C.4:1 D.5:1
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:选择题
一定条件下用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列正确的选项是(NA代表阿伏加德罗常数值)( )
A.CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(l) ΔH=-867 kJ·mol-1
B.CH4催化还原NOx为N2的过程中,若x=1.6,则转移电子3.2NA
C.若0.2molCH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
D.若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移电子3.2NA
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:实验题
已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷。为了探究甲烷性质,某同学设计如下两组实验方案:
甲方案探究甲烷与氧化剂反应(如图1所示);
乙方案探究甲烷与氯气反应的条件(如图2所示)。
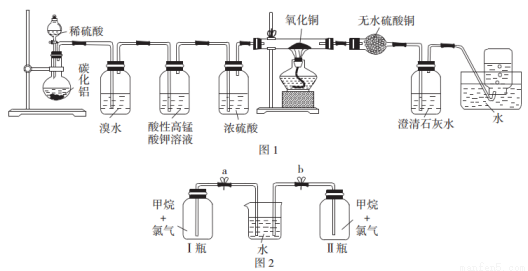
甲方案实验现象:溴水不褪色,无水硫酸铜变蓝色,澄清石灰水变浑浊。
乙方案实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1:4)的混合气体,I瓶放在光亮处,Ⅱ瓶用预先准备好的黑色纸套套上,按图2安装好装置,并加紧弹簧夹a和b。
(1)碳化铝与稀硫酸反应的化学方程式为____________________。
(2)实验甲中浓硫酸的作用是_______________,集气瓶中收集到的气体_________(填“能”或“不能”)直接排入空气中。
(3)下列对甲方案实验中的有关现象与结论的叙述都正确的是_________(填标号)。
A.酸性高锰酸钾溶液不褪色,结论是通常条件下甲烷不能与强氧化剂反应
B.硬质玻璃管里黑色粉末无颜色变化,结论是甲烷不与氧化铜反应
C.硬质玻璃管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应
(4)写出甲方案实验中硬质玻璃管里可能发生反应的化学方程式:________________(假设消耗甲烷与氧化铜的物质的量之比为2:7)。
(5)一段时间后,观察到图2装置中出现的实验现象是____________________;然后打开弹簧夹a、b,观察到的实验现象是______________________。
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:推断题
A、B、C、D、E、F六种短周期主族元素的原子序数依次增大。A是元素周期表中原子半径最小的元素;B元素的原子最外层电子数是次外层电子数的2倍;D与A能形成两种原子个数比分别为1:1和1:2的共价化合物X和Y;D还能与E形成两种原子个数比分别为1:1和1:2的离子化合物M和N;F的最高正化合价为+6。
回答下列问题:
(1)C元素的化学名称为____________,F元素的化学名称为____________。
(2)Y的电子式为____________,M中阴离子的离子符号为___________。
(3)由以上六种元素中的两种原子构成的五核10e-分子的空间构型是______________。
(4)用电子式表示化合物E2F的形成过程为____________________。
(5)D、F的简单氢化物的沸点高低为____________(用化学式表示)。
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:填空题
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+ N2O4(l)=3N2(g)+4H2O(g) △H4=- 1048.9kJ/mol
上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_____________________。
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:实验题
将V1mL 1.0 mol.L-1 HC1溶液和V2 ml未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图甲所示(实验中始终保持Vl+V2=50)。回答下列问题:
(1)该实验表明此反应__________(填“吸收”或“释放”)能量,即________能可以转化为__________能;做该实验时,环境温度__________(填“高于”、“低于”或“等于”)22℃。
(2)根据图甲计算该NaOH溶液的浓度约是__________mol.L-l。

(3)如图乙所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质:
①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体
其中能使a端液面高于b端液面的是________(填序号)。
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:填空题
砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题:
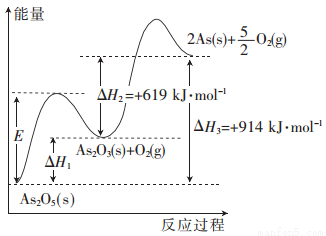
(1)As2O5分解生成As2O3和O2的反应中,加入催化剂,E__________(填“增大”、“减小”或 “不变”,下同),△H1_________。
(2)As2O3分解生成As和O2的热化学方程式为____________________。
(3)As2O3和O2反应生成As2O5的热化学方程式为_____________________。
(4)若1 mol As2O5分解生成0.4 mol As2O3和1.2 mol As,则该分解过程中,需吸收的总能量为_________kJ。
查看答案和解析>>
科目: 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:填空题
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:①CaCO3 (s)=CaO(s)+CO2 (g) △H= -180 kJ·mol-l;
②2CO(g)+SO2(g)=S(s)+2CO2 (g) △H= -270 kJ·mol-l
当反应②放出135 kJ热量时,处理的SO2质量为____________;若该反应放出的热量全部用于煅烧石灰石,则处理SO2时生成CO2与煅烧石灰石时生成的CO2的质量比为___________
(2)已知:CH4(g)+4NO2( g)=4NO(g)+CO2(g)+2H2O(g) △H= -560 kJ·mol-l;
CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H=-1160 kJ·mol-1;
① 若用标准状况下4.48 L CH4还原NO2生成N2,反应中转移的电子总数为_________,(用NA表示阿伏加德罗常数值),放出的热量为_________kJ。
②若1 mol CH4还原NO2时放出的热量为710 kJ,则生成的N2和NO的物质的量之比为____________。
查看答案和解析>>
科目: 来源:2016-2017学年吉林省高二上学期9月月考化学试卷(解析版) 题型:选择题
下列有关化学电池的说法中正确的是( )
A.化学电池只能将化学能转化为电能
B.燃料电池能将全部化学能转化为电能
C.锌银电池比能量大,电压稳定,储存时间长
D.一次电池包括干电池和蓄电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com