
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
化学在生产、生活中应用广泛,下列说法正确的是
A.晶体硅是良好的半导体材料
B.铁、铝合金的熔点高于铁的熔点,硬度小
C.氨常用作制冷剂利用了氨的化学性质
D.漂白粉、明矾都可用于污水的净化,其原理是相同的
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值。下列有关叙述正确的是
A.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
B.1 molN2与4 mol H2反应生成的NH3分子数为2NA
C.1 molFe溶于过量硝酸,电子转移数为2NA
D.34g H2O2和H2S混合物中的氢原子数为2NA
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列离子反应方程式正确的是
A.氯气溶于水:Cl2+H2O═2H++ Cl﹣+ClO-
B.Fe2+与NO3-在酸性溶液中的反应: Fe2++NO3-+4H+=Fe3++NO↑+2H2O
C.稀硫酸和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.浓 硝酸中加入铜片: Cu+4H++2NO3-═Cu2++2NO2↑+2H2O
硝酸中加入铜片: Cu+4H++2NO3-═Cu2++2NO2↑+2H2O
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列实验操作错误的是( )
A. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B. 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C. 用酒精萃取碘水中的碘
D. 配制浓H2SO4和浓HNO3的混酸时,应将H2SO4慢慢加到浓HNO3中,并及时搅拌和冷却
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
O2F2可以发生反应:H2S+4O2F2=SF6+2HF+4O2,下列说法正确的是
A.氧气是氧化产物
B.还原剂与氧化剂的物质的量之比为1:4
C.若生成4.48 L HF,则转移0.8 mol电子
D.O2F2既是氧化剂又是还原剂
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
X、Y、Z、W是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的金属性最强,W原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是
A. X、Y、Z形成的化合物不止一种
B. X的氢化物比Y的氢化物稳定
C. 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X)
D. Y与Z或W形成的化合物中只含离子键
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
用试剂制备下列气体和性质实验中,由现象得出的结论错误的是
选项 | 试剂 | 试纸或试液或气体 | 现象 | 结论 |
A | 浓氨水、生石灰 | 湿润的红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
B | 亚硫酸钠、浓硫酸 | 澄清石灰水溶液 | 溶液先变浑浊后又澄清 | 溶解度 |
C | 浓盐酸、MnO2加热 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
D | 稀硝酸、铜 | 产生无色气体通入空气 | 气体变为 | 无色气体为NO |
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:实验题
以下是有关SO2、Cl2的性质实验。
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
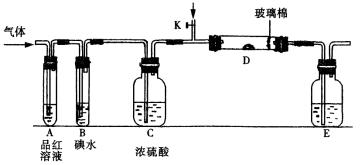
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若D中盛铜粉,通入足量的Cl2,D中的现象是___________;若装置D中装的是五氧化二钒(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
②SO2通入B中,碘水褪色,则该反应的离子方程式为 。
③E中盛有______________溶液。
某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) ,则可以看到白色沉淀产生。
A.氨水 B.硝酸钠溶液 C.氯化钙溶液
若由元素S和O组成–2价酸根离子X,X中S和O的质量比为4∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:实验题
某工厂的废金属屑的主要成分为铝、铁和铜,某化学兴趣小组在学习了元素及其化合物的相关知识后,设计了如图1实验流程,用该工厂的金属废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
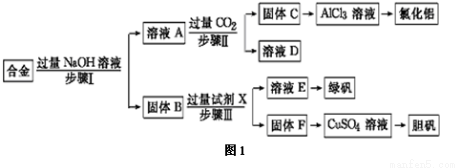
请回答:
(1)铝在周期表中位于 周期 族。
(2)步骤Ⅰ进行的实验操作的名称是 。
(3)写出步骤Ⅱ反应中生成C的离子方程式: 。
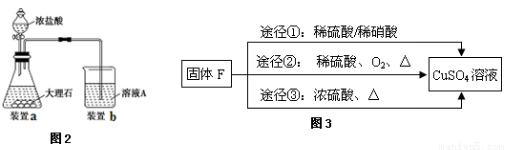
(4)进行步骤Ⅱ时,该小组 用如图2所示装置及试剂制取CO2并将制得的气体通入溶液A中一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少,原因是 。
(5)用固体F制备CuSO4溶液,可设计如图3三种途径:
写出途径③中反应的化学方程式: ,用途径①制备CuSO4溶液时,混酸中硫酸和硝酸的最佳物质的量之比为 。
(6)用途径②制备CuSO4溶液与途径①、③相比优点是 。
查看答案和解析>>
科目: 来源:2017届四川省高三上学期10月月考化学试卷(解析版) 题型:填空题
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl2液中需加入少量铁属,其目的是 。
(2)甲组同学取2mlFeCl2溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为___________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5ml煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是 。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二只试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有__________(填离子符号),由此可以证明该氧化还原反应为__________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液·变成棕黄色,发生反应的离子方程式为________ ;一段时间后.溶液中有气泡出现,并放热.随后有红褐色沉淀生成。产生气泡的原因是__________;生成沉淀的原因是__________(用平衡移动原理解释)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com